Efecto anomérico
En química orgánica, el efecto anomérico o efecto Edward-Lemieux es un efecto estereoelectrónico que describe la tendencia de los sustituyentes heteroatómicos adyacentes a un heteroátomo en un anillo de ciclohexano a preferir la orientación axial en vez de la orientación ecuatorial menos cubierta, que se esperaría a partir de consideraciones estéricas.[1] Este efecto fue observado originalmente en anillos de piranosa por J. T. Edward en 1955; en aquel tiempo, N.-J. Chii y Raymond U. Lemieux comenzaron a estudiar el equilibrio de anomerización de los derivados totalmente acetilados de algunas aldohexopiranosas. El término "efecto anomérico" fue introducido en 1958.[2] El efecto anomérico obtuvo su nombre a partir del término usado para designar el carbono C-1 de una piranosa, el carbono anomérico. Los isómeros que difieren sólo en la configuración del carbono anomérico son denominados anómeros
El efecto anomérico puede ser generalizado a cualquier sistema con la fórmula general R-Y-C-Z, donde Y es un átomo con uno o más pares libres de electrones, y Z es un átomo de alta electronegatividad. La magnitud del efecto anomérico se estima de 1-2 kcal/mol en el caso de los azúcares. En este caso general, la molécula no necesita ser cíclica. Por ejemplo, una molécula pequeña que exhiba el efecto anomérico y suele ser usada para estudios teóricos es el dimetoximetano. En el caso del dimetoxietano, el confórmero gauche tiene una energía 3-5 kcal/mol menor en energía (por tanto, más estable) que la conformación trans: aproximadamente dos veces tan grande como el efecto en los azúcares, porque hay dos enlaces capaces de rotar que son afectados.
Orígenes físicos[editar]
Se han propuesto algunas explicaciones para el efecto anomérico.
La explicación más simple es que la configuración ecuatorial tiene los dipolos de ambos heteroátomos parcialmente alineados, y por tanto repeliéndose mutuamente. En contraste, la configuración axial tiene los dipolos aproximadamente opuesto, representando entonces un estado de menor energía y más estable.

En 1989, los estudios de modelamiento molecular de Box sobre los sacáridos, y el análisis de la información cristalográfica del Cambridge Crystallographic Database usando mecánica molecular basada en el programa STR3DI32, condujeron a un refinamiento de la hipótesis dipolar al mostrar que las repulsiones dipolares originalmente sugeridas, estaban reforzadas por enlaces de hidrógeno C-H···O significativos, estabilizantes, que involucran al grupo funcional acetal.[3] Cálculos de orbitales moleculares más recientes son consistentes con esta hipótesis.[4] Este análisis más comprensivo de los orígenes del efecto anomérico ha llevado también a un mejor entendimiento del efecto anomérico reverso, relacionado al primero e igualmente confuso.[5]
Una explicación alternativa y ampliamente aceptada es que hay una interacción de estabilización (hiperconjugación) entre el par electrónico no compartido de un heteroátomo ( el átomo endocíclico en un anillo de azúcar) y el orbital σ* del enlace axial (exocíclico) C-X. Cuando el átomo exocíclico (en un azúcar) lleva un par libre de electrones, debe haber una interacción similar entre el par de electrones no compartido (del átomo exocíclico) y el orbital σ* del enlace C-O anular. Esta segunda interacción, que es una característica fuerte del anómero β(grupo exocíclico ecuatorial) debería atenuar significativamente el efecto anomérico. Sin embargo, es bien conocido que cuando el átomo exocíclico lleva pares libres de electrones, el efecto anomérico es máximo.
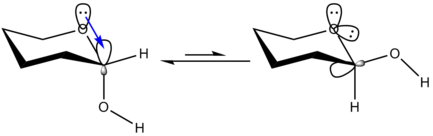
Algunos autores también cuestionan la validez de este modelo, basándose en los resultados de la teoría de los átomos en las moléculas.[6]
Aunque la mayoría de los estudios sobre los efectos anoméricos han sido de naturaleza teórica, la hipótesis n–σ* ha sido extensamente criticada en base que la redistribución de la densidad electrónica en los acetales, propuesta por esta hipótesis, no es congruente con la química experimental conocida de los acetales y, en particular, la química de los monosacáridos.[7][8]
Véase también[editar]
Referencias[editar]
- ↑ Unión Internacional de Química Pura y Aplicada (1996). «Anomeric Effect». Compendium of Chemical Terminology. Versión en línea (en inglés).
- ↑ Juaristi, E.; Cuevas, G. (1992). «Recent studies of the anomeric effect». Tetrahedron 48: 5019-5087. doi:10.1016/S0040-4020(01)90118-8.
- ↑ Box, V. G. S. (1998). «The anomeric effect of monosaccharides and their derivatives. Insights from the new QVBMM molecular mechanics force field». Heterocycles 48 (11): 2389-2417. doi:10.3987/REV-98-504.
- ↑ Takahashi, O.; Yamasaki, K.; Hohno, Y.; Ohtaki, R.; Ueda, K.; Suezawa, H.; Umezawa, Y.; Nishio, M. (2007). «The anomeric effect revisited. A possible role of the CH/n hydrogen bond». Carbohydr. Res. 342: 1202-1209. doi:10.1016/j.carres.2007.02.032.
- ↑ Box, V. G. S. (2000). «Explorations of the Origins of the Reverse Anomeric Effect of the Monosaccharides using the QVBMM (Molecular Mechanics) Force Field». J. Mol. Struct. 522: 145-164. doi:10.1016/S0022-2860(99)00358-0.
- ↑ Vila, A.; Mosquera, R. A. (2007). «Atoms in molecules interpretation of the anomeric effect in the O—C—O unit». J. Comp. Chem. 28: 1516-1530. doi:10.1002/jcc.20585.
- ↑ Box, V. G. S. (1990). «The role of lone pair interactions in the chemistry of the monosaccharides. The anomeric effect». Heterocycles 31: 1157-1181.
- ↑ Box, V. G. S. (1991). «The role of lone pair interactions in the chemistry of the monosaccharides. Stereo-electronic effects in unsaturated monosaccharides». Heterocycles 32: 795-807. doi:10.3987/REV-91-425.
