Vulcanización con azufre

La vulcanización con azufre es un proceso químico para convertir caucho natural o polímeros relacionados en materiales de una variedad de dureza, elasticidad y durabilidad mecánica calentándolos con azufre[1] u otros curativos o aceleradores equivalentes.[2] El azufre forma puentes de reticulación entre secciones de cadenas de polímeros que afectan las propiedades mecánicas y electrónicas. Muchos productos están hechos con caucho vulcanizado, incluidos neumáticos, suelas de zapatos, mangueras y cintas transportadoras. El término vulcanization se deriva de Vulcan, el dios romano del fuego.
Los principales polímeros sometidos a vulcanización con azufre son el poliisopreno (caucho natural, NR), el caucho de polibutadieno (BR) y el caucho de estireno-butadieno (SBR), todos ricos en enlaces insaturados.[3] También se pueden vulcanizar varios otros cauchos especiales, como caucho de nitrilo (NBR), caucho de butilo (IIR) y caucho EPDM. La vulcanización, al igual que el curado de otros polímeros termoendurecibles, es generalmente irreversible. Sin embargo, importantes esfuerzos se han centrado en desarrollar procesos de "des-vulcanización" para el reciclaje de desechos de caucho.
Detalles estructurales y mecanicistas[editar]

Los detalles de la vulcanización siguen siendo turbios porque el proceso convierte mezclas de polímeros en mezclas de derivados insolubles. Por diseño, la reacción no llega a completarse porque el polímero completamente reticulado sería demasiado rígido para las aplicaciones.[4] Durante mucho tiempo ha habido incertidumbre en cuanto a si la vulcanización se produce de manera radical o iónica.[2]
Se conviene en que los sitios reactivos, a menudo denominados "sitios de curación", son los grupos alilo (-CH=CH-CH2-). El azufre forma un puente entre estos sitios, reticulando las cadenas de polímero. Estos puentes pueden constar de uno o varios átomos de azufre. Tanto el grado de reticulación como el número de átomos de azufre en las reticulaciones influyen fuertemente en las propiedades físicas del caucho producido.[5]
Normalmente, los enlaces cruzados están separados por cientos o miles de carbonos en la cadena del polímero.[4]
- Una reticulación excesiva puede convertir el caucho en una sustancia dura y quebradiza (es decir, ebonita).
- Los enlaces cruzados cortos, que poseen un menor número de átomos de azufre, dan al caucho una mejor resistencia al calor y la intemperie.
- Los enlaces cruzados más largos, con un mayor número de átomos de azufre, dan al caucho una mayor durabilidad física y resistencia a la tracción.
El azufre, por sí mismo, es un agente de vulcanización lenta y no vulcaniza las poliolefinas sintéticas. Incluso con caucho natural, son necesarias grandes cantidades de azufre, así como altas temperaturas y períodos de calentamiento prolongados, siendo los productos finales a menudo de una calidad insatisfactoria.
Desde principios de la década de 1900, se han desarrollado varios aditivos químicos para mejorar la velocidad y eficiencia de la vulcanización, así como para controlar la naturaleza de la reticulación.[6] Cuando se usa en conjunto, esta colección - el "paquete de curado" - da una goma con propiedades particulares.
Paquete de curado[editar]
El paquete de curado consta de varios reactivos que modifican la cinética y la química de la reticulación. Estos incluyen aceleradores, activadores, retardadores e inhibidores.[6][7] Tenga en cuenta que estos son simplemente los aditivos utilizados para la vulcanización y que también se pueden agregar otros compuestos al caucho, como cargas o estabilizadores poliméricos.
Fuente de azufre[editar]
El azufre ordinario (octaazufre) se usa raramente, a pesar de su bajo costo, porque es insoluble en el polímero. A las temperaturas de vulcanización, el azufre se licua y la fase se separa, esta floración de azufre impide la mezcla íntima del polímero y el reticulante. En su lugar, se utilizan varias formas de azufre polimérico. También es posible reemplazar el azufre con otros compuestos donantes de azufre, por ejemplo, aceleradores que llevan grupos disulfuro, en lo que a menudo se denomina "vulcanización eficaz" (EV).[2] También se puede utilizar dicloruro de disulfuro para la "vulcanización en frío".
Acelerantes[editar]
Los acelerantes (aceleradores) actúan de manera muy similar a los catalizadores, lo que permite que la vulcanización se realice de manera más fría, más rápida y con un uso más eficiente del azufre.[2][8] Lo logran al reaccionar con el azufre y romperlo para formar un intermedio reactivo, denominado agente sulfurante. Este, a su vez, reacciona con los sitios de curado del caucho para provocar la vulcanización.
Hay dos clases principales de aceleradores de vulcanización: aceleradores primarios y aceleradores secundarios (también conocidos como ultraaceleradores). Los activadores primarios datan del uso de amoníaco en 1881,[9] mientras que los aceleradores secundarios se han desarrollado alrededor de 1920.[10]
- Primario (aceleradores rápidos)
Los aceleradores primarios realizan la mayor parte de la aceleración y consisten principalmente en tiazoles, a menudo derivatizados con grupos sulfenamida.[11] El compuesto principal es el 2-mercaptobenzotiazol (MBT), que se utiliza desde la década de 1920.[12] Sigue siendo un agente de curado moderadamente rápido que da cadenas de azufre de longitud media, pero su período de inducción relativamente corto puede ser una desventaja. Otros aceleradores primarios son esencialmente formas "enmascaradas" de MBT, que necesitan tiempo para descomponerse en MBT durante la vulcanización y, por lo tanto, tienen períodos de inducción más largos.
-
Mercaptobenzotiazol (MBT)
-
Disulfuro de mercaptobenzotiazol (MBTS)
-
Diciclohexil-2-benzotiazolesulfenamida (DCBS)
La dimerización oxidativa de MBT da disulfuro de mercaptobenzotiazol (MBTS), y los derivados de sulfenamida se producen haciendo reaccionar esto con aminas primarias como ciclohexilamina o terc-butilamina. Se pueden usar aminas secundarias como diciclohexilamina y dar como resultado aceleradores aún más lentos. Se requiere un acelerante lento de este tipo en aplicaciones en las que el caucho se cura sobre un componente metálico al que se requiere adherir, como los cordones de acero en los neumáticos de vehículos.
- Secundario (ultraacelerantes)
Los aceleradores secundarios o ultraaceleradores se utilizan en pequeñas cantidades para aumentar el comportamiento de los aceleradores primarios. Actúan para aumentar la velocidad de curado y aumentar la densidad del entrecruzamiento, pero también acortan el tiempo de inducción, lo que puede provocar una vulcanización prematura.[6] Químicamente, consisten principalmente en especies de tiocarbonilo tales como tiurams, ditiocarbamatos, xantatos y tioureas orgánicas; también se utilizan guanidinas aromáticas. Estos compuestos deben combinarse con activadores, generalmente iones de zinc, para que sean completamente activos.
-
difenilguanidina (DPG)
Los aceleradores secundarios tienen velocidades de vulcanización muy rápidas con un tiempo de inducción mínimo, lo que los hace inadecuados como aceleradores primarios en cauchos altamente insaturados como NR o SBR. Sin embargo, se pueden utilizar como aceleradores primarios en compuestos con menos sitios de curado como EPDM. Los xantatos (principalmente, xantato de isopropilo de zinc) son importantes en la vulcanización del látex, que se cura a una temperatura relativamente baja (100-120 °C) y, por lo tanto, necesita un acelerador intrínsecamente rápido. Los principales tiurams utilizados son TMTD (disulfuro de tetrametiltiuram) y TETD (disulfuro de tetraetiltiuram). Los principales ditiocarbamatos son las sales de zinc ZDMC (dimetilditiocarbamato de zinc), ZDEC (dietilditiocarbamato de zinc) y ZDBC (dibutilditiocarbamato de zinc).
Activadores[editar]
Los activadores consisten en varias sales metálicas, ácidos grasos y bases que contienen nitrógeno, siendo las más importantes el óxido de zinc. El zinc activa muchos aceleradores por coordinación, por ejemplo, haciendo que el tiuram se convierta en ziram.[13] El zinc también se coordina con las cadenas de azufre de los agentes sulfurantes, cambiando el enlace más probable que se rompa durante la formación del entrecruzamiento. En última instancia, los activadores promueven el uso eficiente del azufre para proporcionar una alta densidad de enlaces cruzados.[14] Debido a la baja solubilidad del ZnO, a menudo se combina con ácidos grasos como el ácido esteárico para formar un jabón metálico más soluble, es decir, estearato de zinc.
Retardadores e inhibidores[editar]
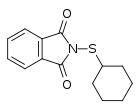
Para garantizar una vulcanización de alta calidad, el caucho, el azufre, los acelerantes, los activadores y otros compuestos se mezclan para obtener una mezcla homogénea. En la práctica, la mezcla puede resultar en la fusión del azufre (punto de fusión 115 °C para S8). A estas temperaturas, la vulcanización puede comenzar prematuramente, lo que a menudo es indeseable, ya que la mezcla puede necesitar ser bombeada y moldeada en su forma final antes de solidificarse. La vulcanización prematura a menudo se denomina "chamuscado". El quemado se puede prevenir mediante el uso de retardadores o inhibidores, que aumentan el período de inducción antes de que comience la vulcanización y, por lo tanto, proporcionan resistencia al quemado. Un retardador ralentiza tanto el inicio como la velocidad de vulcanización, mientras que los inhibidores solo retrasan el inicio de la vulcanización y no afectan la velocidad en gran medida.[15] En general, se prefieren los inhibidores, con ciclohexiltioftalimida (a menudo denominada PVI - inhibidor de pre-vulcanización) siendo el ejemplo más común.
Desvulcanización[editar]
El mercado de caucho en bruto nuevo o equivalente es grande. La industria automotriz consume una fracción sustancial de caucho natural y sintético. El caucho recuperado tiene propiedades alteradas y no es adecuado para su uso en muchos productos, incluidos los neumáticos. Los neumáticos y otros productos vulcanizados son potencialmente susceptibles de desvulcanización, pero esta tecnología no ha producido material que pueda suplantar a los materiales no vulcanizados. El principal problema es que los enlaces carbono-azufre no se rompen fácilmente sin la entrada de costosos reactivos y calor. Por tanto, más de la mitad de la goma de desecho se quema simplemente como combustible.[16]
Vulcanización inversa[editar]
Aunque el azufre polimérico vuelve a su monómero a temperatura ambiente, los polímeros que consisten principalmente en azufre se pueden estabilizar con enlazadores orgánicos como el 1,3-diisopropenilbenceno.[17] Este proceso se llama vulcanización inversa y produce polímeros donde el azufre es el componente principal.[18]
Historia[editar]
El curado del caucho se lleva a cabo desde tiempos prehistóricos.[19] El nombre de la primera civilización importante en Guatemala y México, el olmeca, significa 'pueblo de goma' en el idioma azteca. Los antiguos mesoamericanos, desde los antiguos olmecas hasta los aztecas, extraían látex de Castilla elástica, un tipo de árbol de caucho de la zona. El jugo de una vid local, Ipomoea alba, se mezcló con este látex para crear caucho procesado ya en 1600 a. C.[20] En el mundo occidental, el caucho siguió siendo una curiosidad, aunque finalmente se utilizó para producir productos impermeabilizados, como la ropa impermeable Mackintosh, a principios del siglo XIX.[21]
Desarrollos modernos[editar]
En 1832-1834, Nathaniel Hayward y Friedrich Ludersdorf descubrieron que el caucho tratado con azufre perdió su pegajosidad. Es probable que Hayward compartiera su descubrimiento con Charles Goodyear, posiblemente inspirándolo a hacer el descubrimiento de la vulcanización.[22]
Thomas Hancock (1786–1865), científico e ingeniero, fue el primero en patentar la vulcanización del caucho. Se le concedió una patente británica el 21 de mayo de 1845. Tres semanas después, el 15 de junio de 1845, Charles Goodyear obtuvo una patente en los Estados Unidos.[23] Fue el amigo de Hancock, William Brockedon, quien acuñó el término "vulcanización".[24]
Goodyear afirmó que había descubierto la vulcanización antes, en 1839. Escribió la historia del descubrimiento en 1853 en su libro autobiográfico Gum-Elastica. Aquí está el relato de Goodyear de la invención, tomado de Gum-Elastica. Aunque el libro es una autobiografía, Goodyear optó por escribirlo en tercera persona. Describe la escena en una fábrica de caucho donde trabajaba su hermano:
El inventor realizó experimentos para determinar el efecto del calor sobre el mismo compuesto que se había descompuesto en las bolsas de correo y otros artículos. Se sorprendió al descubrir que el espécimen, al entrar descuidadamente en contacto con una estufa caliente, estaba carbonizado como el cuero.
Goodyear continúa describiendo cómo su descubrimiento no fue aceptado fácilmente.
Él infirió directamente que si el proceso de carbonización pudiera detenerse en el punto correcto, podría despojar a la goma de su adhesividad nativa en todas partes, lo que la haría mejor que la goma nativa. Tras una nueva prueba con calor, se convenció aún más de la exactitud de esta inferencia al descubrir que el caucho de la India no se podía fundir en azufre hirviendo a ningún calor, sino que siempre se carbonizaba. Hizo otra prueba de calentar una tela similar ante un fuego abierto. Siguió el mismo efecto, el de quemar la goma de mascar. Hubo más indicios de éxito en la producción del resultado deseado, ya que en el borde de la porción carbonizada apareció una línea o borde, que no estaba carbonizado, sino perfectamente curado.
Goodyear luego describe cómo se mudó a Woburn, Massachusetts y llevó a cabo una serie de experimentos sistemáticos para optimizar el curado del caucho, en colaboración con Nathaniel Hayward.
Al comprobar con certeza que había encontrado el objeto de su búsqueda y mucho más, y que la nueva sustancia era resistente al frío y al solvente de la goma nativa, se sintió ampliamente recompensado por el pasado, y bastante indiferente a futuras pruebas.
Desarrollos posteriores[editar]
El descubrimiento de la reacción caucho-azufre revolucionó el uso y las aplicaciones del caucho, cambiando la faz del mundo industrial. Anteriormente, la única forma de sellar un pequeño espacio entre las partes móviles de la máquina era usar cuero empapado en aceite. Esta práctica era aceptable solo a presiones moderadas, pero por encima de cierto punto, los diseñadores de máquinas se vieron obligados a comprometerse entre la fricción adicional generada por un empaque más apretado y una mayor fuga de vapor. El caucho vulcanizado resolvió este problema. Se podía formar con formas y dimensiones precisas, aceptaba deformaciones de moderadas a grandes bajo carga y se recuperaba rápidamente a sus dimensiones originales una vez que se retiraba la carga. Estas cualidades excepcionales, combinadas con una buena durabilidad y falta de adherencia, fueron críticas para un material de sellado eficaz. Otros experimentos de Hancock y sus colegas en el procesamiento y la composición del caucho llevaron a un proceso más confiable.
Alrededor de 1900, se introdujo el disulfiram como agente vulcanizante y se volvió ampliamente utilizado.[25]
En 1905, George Oenslager descubrió que un derivado de la anilina llamado tiocarbanilida aceleraba la reacción del azufre con el caucho, lo que reducía los tiempos de curado y reducía el consumo de energía. Este avance fue casi tan fundamental para la industria del caucho como el curado por azufre de Goodyear. Los aceleradores aceleraron el proceso de curado, mejoraron la confiabilidad del proceso y permitieron aplicar la vulcanización a los polímeros sintéticos. Un año después de su descubrimiento, Oenslager había encontrado cientos de aplicaciones para su aditivo. Así nació la ciencia de los aceleradores y retardadores. Un acelerador acelera la reacción de curado, mientras que un retardador la retrasa. Un retardador típico es la ciclohexiltioftalimida. En el siglo siguiente, los químicos desarrollaron otros aceleradores y ultraaceleradores, que se utilizan en la fabricación de la mayoría de los productos de caucho modernos.
Referencias[editar]
- ↑ James E. Mark, Burak Erman (eds.) (2005). Science and technology of rubber. p. 768. ISBN 978-0-12-464786-2.
- ↑ a b c d Akiba, M (1997). «Vulcanization and crosslinking in elastomers». Progress in Polymer Science 22 (3): 475-521. doi:10.1016/S0079-6700(96)00015-9.
- ↑ Coran, A.Y. (2013). «Chapter 7 - Vulcanization». The science and technology of rubber (Fourth edición). Elsevier. pp. 337-381. ISBN 978-0-12-394584-6. doi:10.1016/B978-0-12-394584-6.00007-8.
- ↑ a b Coran, A. Y. (3 de enero de 2003). «Chemistry of the vulcanization and protection of elastomers: A review of the achievements». Journal of Applied Polymer Science 87 (1): 24-30. doi:10.1002/app.11659.
- ↑ Nasir, M.; Teh, G.K. (January 1988). «The effects of various types of crosslinks on the physical properties of natural rubber». European Polymer Journal 24 (8): 733-736. doi:10.1016/0014-3057(88)90007-9.
- ↑ a b c d Engels, Hans-Wilhelm; Weidenhaupt, Herrmann-Josef; Pieroth, Manfred; Hofmann, Werner; Menting, Karl-Hans; Mergenhagen, Thomas; Schmoll, Ralf; Uhrlandt, Stefan (2011). Rubber, 9. Chemicals and Additives. ISBN 978-3527306732. doi:10.1002/14356007.a23_365.pub3.
- ↑ Aprem, Abi Santhosh; Joseph, Kuruvilla; Thomas, Sabu (July 2005). «Recent Developments in Crosslinking of Elastomers». Rubber Chemistry and Technology 78 (3): 458-488. doi:10.5254/1.3547892.
- ↑ Hewitt, Norman; Ciullo, Peter A. (1999). «Compounding Materials». The rubber formulary. Noyes Publications. pp. 4–49. ISBN 9780815514343. doi:10.1016/B978-081551434-3.50003-8.
- ↑ Geer, W. C.; Bedford, C. W. (April 1925). «The History of Organic Accelerators in the Rubber Industry.». Industrial & Engineering Chemistry 17 (4): 393-396. doi:10.1021/ie50184a021.
- ↑ Whitby, G. Stafford. (October 1923). «Accelerators of Vulcanization.». Industrial & Engineering Chemistry 15 (10): 1005-1008. doi:10.1021/ie50166a007.
- ↑ Koval', I V (1996). «Synthesis and application of sulfenamides». Russian Chemical Reviews 65 (5): 421-440. Bibcode:1996RuCRv..65..421K. doi:10.1070/RC1996v065n05ABEH000218.
- ↑ Sebrei, L. B.; Boord, C. E. (October 1923). «1-Mercaptobenzothiazole and Its Derivatives as Accelerators of Rubber Vulcanization.». Industrial & Engineering Chemistry 15 (10): 1009-1014. doi:10.1021/ie50166a009.
- ↑ Nieuwenhuizen, P. J.; Reedijk, J.; van Duin, M.; McGill, W. J. (July 1997). «Thiuram- and Dithiocarbamate-Accelerated Sulfur Vulcanization from the Chemist's Perspective; Methods, Materials and Mechanisms Reviewed». Rubber Chemistry and Technology 70 (3): 368-429. doi:10.5254/1.3538436.
- ↑ Nieuwenhuizen, Peter J.; Ehlers, Andreas W.; Haasnoot, Jaap G.; Janse, Sander R.; Reedijk, Jan; Baerends, Evert Jan (January 1999). «The Mechanism of Zinc(II)-Dithiocarbamate-Accelerated Vulcanization Uncovered; Theoretical and Experimental Evidence». Journal of the American Chemical Society 121 (1): 163-168. doi:10.1021/ja982217n.
- ↑ Sadhan K. De; Jim R. White (2001). Rubber Technologist's Handbook. iSmithers Rapra Publishing. pp. 184-. ISBN 978-1-85957-262-7.
- ↑ Myhre, Marvin; MacKillop, Duncan A (2002). «Rubber Recycling». Rubber Chemistry and Technology 75 (3): 429-474. doi:10.5254/1.3547678.
- ↑ Chung, Woo Jin; Griebel, Jared J.; Kim, Eui Tae; Yoon, Hyunsik; Simmonds, Adam G.; Ji, Hyun Jun; Dirlam, Philip T.; Glass, Richard S. et al. (2013). «The Use of Elemental Sulfur as an Alternative Feedstock for Polymeric Materials». Nature Chemistry 5 (6): 518-524. Bibcode:2013NatCh...5..518C. PMID 23695634. doi:10.1038/nchem.1624.
- ↑ Boyd, Darryl A. (2016). «Sulfur and Its Role In Modern Materials Science». Angewandte Chemie International Edition 55 (50): 15486-15502. PMID 27860133. doi:10.1002/anie.201604615.
- ↑ Hosler, D. (18 de junio de 1999). «Prehistoric Polymers: Rubber Processing in Ancient Mesoamerica». Science 284 (5422): 1988-1991. PMID 10373117. doi:10.1126/science.284.5422.1988.
- ↑ D Hosler, SL Burkett and MJ Tarkanian (1999). «Prehistoric Polymers: Rubber Processing in Ancient Mesoamerica». Science 284 (5422): 1988-1991. PMID 10373117. doi:10.1126/science.284.5422.1988.
- ↑ «Whonamedit – James Syme». Whonamedit. Consultado el 23 de agosto de 2013.
- ↑ Saccomandi, Giuseppe; Ogden, Raymond W. (4 de mayo de 2014). Mechanics and Thermomechanics of Rubberlike Solids. ISBN 9783709125403.
- ↑ 1493: Uncovering the New World Columbus Created. Random House Digital, Inc. 2011. pp. 244-245. ISBN 9780307265722.
- ↑ Fisher, Harry L. (November 1939). «VULCANIZATION OF RUBBER Vulcanization of Rubber». Industrial & Engineering Chemistry 31 (11): 1381-1389. doi:10.1021/ie50359a015.
- ↑ Kragh, Helge (2008). «From Disulfiram to Antabuse: The Invention of a Drug». Bulletin for the History of Chemistry 33 (2): 82-88.




