Disolución

Una disolución es una mezcla homogénea a nivel molecular o iónico de dos o más sustancias puras que no reaccionan entre sí, cuyos componentes se encuentran en proporciones variables.[1][2] También se puede definir como una mezcla homogénea formada por un disolvente y por uno o varios solutos.
Un ejemplo común podría ser un sólido disuelto en un líquido, como la sal o el azúcar disueltos en agua; o incluso el oro en mercurio, formando una amalgama. También otros ejemplos de disoluciones son el vapor de agua en el aire, el hidrógeno en paladio o cualquiera de las aleaciones existentes.
El término también es usado para hacer referencia al proceso de disolución. De acuerdo con Jöns Jacob Berzelius, la diferencia entre solución y disolución fue señalada por Antoine Lavoisier.[3]
Disolvente y soluto
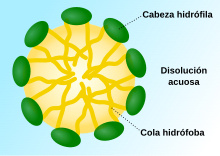
Una disolución es una mezcla homogénea de sustancias puras. Frecuentemente formada por un solvente, disolvente, dispersante o medio de dispersión, medio en el que se disuelven los solutos, y uno o varios solutos. Los criterios para decidir cuál es el disolvente y cuáles los solutos son más o menos arbitrarios; no hay una razón científica para hacer tal distinción.[4]
Wilhelm Ostwald distingue tres tipos de mezclas según el tamaño de las partículas de soluto en la disolución:[5]
- Dispersiones, suspensiones o falsas disoluciones: cuando el diámetro de las partículas de soluto excede de 0,1 μm.
- Dispersoides, coloides: el tamaño está entre 0,001 μm y 0,1 μm.
- Dispérsidos o disoluciones verdaderas: el tamaño es menor a 0,001 μm.
Estas últimas se clasifican en:
- Disoluciones con condensación molecular: la partícula dispersa está formada por una condensación de moléculas.
- Disoluciones moleculares: cada partícula es una molécula.
- Disoluciones iónicas: la partícula dispersa es un ion (fracción de molécula con carga eléctrica).
- Disoluciones atómicas: cada partícula dispersa es un átomo.
Características generales
- Son mezclas homogéneas: las proporciones relativas de solutos y solvente se mantienen en cualquier cantidad que tomemos de la disolución (por pequeña que sea la gota), y no se pueden separar por centrifugación ni filtración.
- La disolución consta de dos partes: soluto y disolvente.
- Cuando el soluto se disuelve, éste pasa a formar parte de la disolución.
- Al disolver una sustancia, el volumen final es diferente a la suma de los volúmenes del disolvente y el soluto, debido a que los volúmenes no son aditivos.[6]
- La cantidad de soluto y la cantidad de disolvente se encuentran en proporciones variables entre ciertos límites. Normalmente el disolvente se encuentra en mayor proporción que el soluto, aunque no siempre es así. La proporción en que tengamos el soluto en el seno del disolvente depende del tipo de interacción que se produzca entre ellos. Esta interacción está relacionada con la solubilidad del soluto en el disolvente, es decir, tiene que ver con la cantidad de soluto que es capaz de admitir este disolvente.
- Las propiedades físicas de la solución son diferentes a las del solvente puro: la adición de un soluto a un solvente aumenta su punto de ebullición y disminuye su punto de congelación; la adición de un soluto a un solvente disminuye la presión de vapor de éste.
- Sus propiedades físicas dependen de su concentración:
- Disolución HCl 12 mol/L; densidad = 1,18 g/cm³
- Disolución HCl 6 mol/L; densidad = 1,10 g/cm³
- Las propiedades químicas de los componentes de una disolución no se alteran.
- Como éstos no se pueden separar por centrifugación o filtración; Sus componentes se obtienen a través de otros métodos conocidos como métodos de fraccionamiento, como es el caso de la destilación o la cristalización.
Tipos de disoluciones
Por su estado de agregación
Sólido
- Sólido en sólido: cuando tanto el soluto como el solvente se encuentran en estado sólido. Un ejemplo claro de este tipo de disoluciones son las aleaciones, como el zinc en el estaño.
- Gas en sólido: un ejemplo es el hidrógeno (gas), que se disuelve bastante bien en metales, especialmente en el paladio (sólido). Esta característica del paladio se estudia como una forma de almacenamiento de hidrógeno.
- Líquido en sólido: cuando una sustancia líquida se disuelve junto con un sólido. Las amalgamas se hacen con mercurio (líquido) mezclado con plata (sólido).
Líquido
- Sólido en líquido: este tipo de disoluciones es de las más utilizadas, pues se disuelven por lo general pequeñas cantidades de sustancias sólidas en grandes cantidades líquidas. Un ejemplo claro de este tipo es la mezcla de agua con azúcar.
- Gas en líquido: por ejemplo, oxígeno en agua o dióxido de azufre en agua.
- Líquido en líquido: esta es otra de las disoluciones más utilizadas. Por ejemplo, diferentes mezclas de alcohol en agua (cambia la densidad final). Un método para volverlas a separar es por destilación.
Gas
- Gas en gas: son las disoluciones gaseosas más comunes. Un ejemplo es el aire (compuesto por oxígeno y otros gases disueltos en nitrógeno). Dado que en estas soluciones casi no se producen interacciones moleculares, las soluciones que los gases forman son bastante triviales. Incluso en parte de la literatura no están clasificadas como soluciones, sino como mezclas.[cita requerida]
- Sólido en gas: no son comunes, pero como ejemplo se pueden citar el yodo sublimado disuelto en nitrógeno[4] y el polvo atmosférico disuelto en el aire.[5]
- Líquido en gas: por ejemplo, el aire húmedo.[4]
Ejemplo
A continuación se presenta un cuadro con ejemplos de disoluciones clasificadas por su estado de agregación donde se muestran todas las combinaciones posibles:
| Ejemplos de disoluciones | Soluto | |||
|---|---|---|---|---|
| Gaseoso | Líquido | Sólido | ||
| Disolvente | Gas | El oxígeno y otros gases en nitrógeno (aire). | El vapor de agua en el aire. | La naftalina se sublima lentamente en el aire, entrando en solución. |
| Líquido | El dióxido de carbono en agua, formando agua carbonatada. Las burbujas visibles no son el gas disuelto, sino solamente una efervescencia. El gas disuelto en sí mismo no es visible en la solución. | El etanol (alcohol común) en agua; varios hidrocarburos el uno con el otro (petróleo). | La sacarosa (azúcar de mesa) en agua; el cloruro de sodio (sal de mesa) en agua; oro en mercurio, formando una amalgama. | |
| Sólido | El hidrógeno se disuelve en los metales; el platino ha sido estudiado como medio de almacenamiento. | El hexano en la cera de parafina; el mercurio en oro. | El acero, duraluminio, y otras aleaciones metálicas. | |
Por su concentración

Por su concentración, la disolución puede ser analizada en términos cuantitativos o cualitativos dependiendo de su estado.
Disoluciones empíricas
También llamadas disoluciones cualitativas, esta clasificación no toma en cuenta la cantidad numérica de soluto y disolvente presentes, y dependiendo de la proporción entre ellos se clasifican de la siguiente manera:
- Disolución diluida: es aquella en donde la cantidad de soluto que interviene está en mínima proporción en un volumen determinado.
- Disolución concentrada: tiene una cantidad considerable de soluto en un volumen determinado.
- Disolución insaturada: no tiene la cantidad máxima posible de soluto para una temperatura y presión dadas.
- Disolución saturada: tienen la mayor cantidad posible de soluto para una temperatura y presión dadas. En ellas existe un equilibrio entre el soluto y el disolvente.
- Disolución sobresaturada: contiene más soluto del que puede existir en equilibrio a una temperatura y presión dadas. Si se calienta una solución saturada se le puede agregar más soluto; si esta solución es enfriada lentamente y no se le perturba, puede retener un exceso de soluto pasando a ser una solución sobresaturada. Sin embargo, son sistemas inestables, con cualquier perturbación el soluto en exceso precipita y la solución regresa a ser saturada; esto se debe a que se mezclaron.
Disoluciones valoradas
A diferencia de las empíricas, las disoluciones valoradas cuantitativamente, sí toman en cuenta las cantidades numéricas exactas de soluto y solvente que se utilizan en una disolución. Este tipo de clasificación es muy utilizada en el campo de la ciencia y la tecnología, pues en ellas es muy importante una alta precisión.
Existen varios tipos de disoluciones valoradas:
- Porcentual
- Molar
- Molal
- Normal
Conocimientos aplicados
En función de la naturaleza de solutos y solventes, las leyes que rigen las disoluciones son distintas.
- Sólidos en sólidos: Leyes de las disoluciones sólidas.
- Sólidos en líquidos: Leyes de la solubilidad.
- Sólidos en gases: Movimientos brownianos y leyes de los coloides.
- Líquidos en líquidos: Tensión interfacial.
- Gases en líquidos: Ley de Henry.
Véase también
Referencias
- ↑ Química. Escrito por William S Seese, G William Daub en Google Libros
- ↑ Hein, morris (2011). «3». En Hugo Rivera Oliver, ed. Fundamentos de química 2 (1 edición). Guadalupe, Nuevo León: Cengage Learning Latinoamérica. p. 160. ISBN 978-607-481-493-4. «Página 52».
- ↑ Jöns Jacob Berzelius (1831), Traité de chimie minérale, végétale et animale, p. 327: "...la différence qu'il établit entre la solution et la dissolution; le une pouvant avoir lieu dans toutes les proportions, tandis que l'autre, changeant la nature du corps dissous, n'admet que des proportions fixes et invariables."
- ↑ a b c Cristóbal Valenzuela Calahorro (1995). Química General: Introducción a la química teórica. Universidad de Salamanca. p. 300. ISBN 9788474817836.
- ↑ a b Santiago Burbano de Ercilla, Carlos Gracía Muñoz (2003). Física general. Casa Editorial Mares - Editorial Tebar. p. 335. ISBN 9788495447821.
- ↑ Sandler, Stanley I.(1999).Chemical and Enginering Thermodynamics. Chapter 6.Third Edition.
<ref> definida en las <references> con nombre «phillips» no se utiliza en el texto anterior.Enlaces externos
- IES Aguilar y Cano, de Estepa (Sevilla), ofrece la posibilidad de trabajar las disoluciones.
