Dengue
| Dengue | ||
|---|---|---|
 Mosquito Aedes aegypti, vector del dengue. | ||
| Especialidad | infectología | |
| Síntomas | Fiebre, dolor de cabeza, dolor muscular y articular, erupción cutánea.[1] | |
| Complicaciones | Sangrado, niveles bajos de plaquetas en la sangre , presión arterial peligrosamente baja | |
| Diagnóstico | Detección de anticuerpos contra el virus o su ARN | |
| Prevención | Vacuna contra el dengue , disminución de la exposición a los mosquitos.[2] | |
| Sinónimos | ||
| ||
El dengue es una enfermedad infecciosa causada por el virus del dengue, perteneciente al género flavivirus, que es transmitida por mosquitos, principalmente por el Aedes aegypti. Existen 4 tipos del virus de dengue. La infección causa síntomas gripales, y en ocasiones evoluciona hasta convertirse en un cuadro potencialmente mortal, llamado dengue grave o dengue hemorrágico.[3]
Es una infección muy extendida que se presenta en todas las regiones de clima tropical del planeta, y últimamente en regiones de clima templado con veranos cálidos y húmedos. En los últimos años la transmisión ha aumentado de manera predominante en zonas urbanas y se ha convertido en un importante problema de salud pública. En la actualidad, más de la mitad de la población mundial está en riesgo de contraer la enfermedad. La prevención y el control del dengue dependen exclusivamente de las medidas eficaces de lucha contra el vector transmisor, el mosquito.[4]
El número de casos de dengue ha aumentado dramáticamente desde la década de 1960. De acuerdo con la OMS, en las últimas dos décadas aumentó 8 veces más el número de casos notificados, con una estimación de entre 284 y 528 millones de personas infectadas anualmente.[5] Las primeras descripciones datan de 1779 y su causa viral y la transmisión fueron entendidas a principios del siglo XX. El dengue se ha convertido en un problema mundial desde la Segunda Guerra Mundial y es endémica en más de 110 países. Aparte de la eliminación de los mosquitos, se está trabajando en una vacuna contra el dengue, así como la medicación dirigida directamente al virus.
Historia[editar]



Antigüedad[editar]
La primera referencia de un caso de dengue aparece en una enciclopedia medicinal china publicada en la dinastía Jin (265-420), formalmente editada durante la dinastía Tang en el año 610, y publicada nuevamente durante la dinastía Song del Norte, en el año 992, que describe una especie de “agua envenenada” asociada a insectos voladores, que tras su picadura provocaban unas fiebres muy elevadas.[6][7][8]
El dengue se extendió fuera de África entre los siglos XV y XIX, debido al desarrollo de la marina mercante y la creciente migración de personas, especialmente en los siglos XVIII y XIX, lo que ocasionó que las ciudades portuarias crecieran y se urbanizaran, creando condiciones ideales para el hábitat del mosquito vector, Aedes aegypti. Durante los viajes marítimos, el mosquito se mantenía vivo en los depósitos de agua de las bodegas. De esta forma, tanto el mosquito como el virus se expandieron a nuevas áreas geográficas, causando epidemias separadas por los intervalos dados por los viajes marítimos (10 a 40 años).[9][8] Existen varias descripciones de epidemias durante el siglo XVII, pero el reporte más antiguo de una posible epidemia de dengue data entre los años 1779 y 1780, cuando una epidemia asoló Asia, África y América del norte.[8][10] El primer reporte de caso definitivo data de 1779 y es atribuido a Benjamin Rush, quien acuña el término «fiebre rompehuesos» por los síntomas de mialgias y artralgias.[7]
Siglo XX hasta la actualidad[editar]
En 1906, la transmisión por el mosquito Aedes fue confirmada, y en 1907 el dengue era la segunda enfermedad que se conocía (después de la fiebre amarilla), que era producida por un virus.[10] Más investigaciones científicas de la época, realizadas por John Burton Cleland y Joseph Franklin Siler completaron el conocimiento básico sobre la transmisión de la enfermedad infecciosa.[10] La marcada expansión del dengue durante y posteriormente a la Segunda Guerra Mundial ha sido atribuido a la disrupción ecológica. Esto mismo, ha permitido que diferentes serotipos del virus se hayan extendido a nuevas áreas geográficas, y se haya convertido en una enfermedad emergente y preocupante en nuestro tiempo, por las nuevas formas mortales de fiebre hemorrágica. Estas formas severas de la enfermedad fueron por primera vez reportadas en Filipinas en 1953; en los 70, se había convertido en la mayor causa de mortalidad infantil en el Pacífico y parte de América.[8]
La fiebre hemorrágica y el choque por dengue fueron por primera vez referidas en América Central y Sudamérica en 1981, en personas que habían contraído el serotipo DENV-2, y que ya habían tenido contacto previo con el serotipo DENV-1.[11] A principios de los años 2000, el dengue se ha vuelto la segunda enfermedad más común de las transmitidas por mosquitos, y que afectan a los seres humanos ―después de la malaria―. Actualmente existen alrededor de 40 millones de casos de dengue y varios cientos de miles de casos de dengue hemorrágico cada año. Hubo un brote grave en Río de Janeiro en febrero de 2002 que afectó a alrededor de un millón de personas.[8]
Etimología[editar]
El origen del término «dengue» no está del todo claro. Según una hipótesis viene de la frase en idioma suajili ka-dinga pepo, describiendo esa enfermedad como provocada por un fantasma.[12] Aunque quizás la palabra suajili dinga posiblemente provenga del castellano «dengue» para fastidioso o cuidadoso, describiendo el sufrimiento de un paciente con el típico dolor de huesos del dengue.[13][6]
Epidemiología[editar]
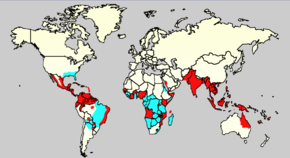

La Organización Mundial de la Salud (OMS) estima que el número de afectados por dengue se encuentra entre los 100 millones y los 400 millones de personas cada año, con un total de medio millón que necesitan atención hospitalaria por presentar una forma grave de la enfermedad, con una mortalidad del 2,5 %.[cita requerida]
Es una enfermedad de aviso epidemiológico.[14][15]
El dengue es conocido como «fiebre rompehuesos», «fiebre quebrantahuesos» y «la quebradora» en países centroamericanos.
Importantes brotes de dengue tienden a ocurrir cada cinco o seis años. Se piensa que la ciclicidad en el número de casos de dengue es el resultado de los ciclos estacionales que interactúan con una corta duración de la inmunidad cruzada para las cuatro cepas en las personas que han tenido el dengue. Cuando la inmunidad cruzada desaparece, entonces la población es más susceptible a la transmisión, sobre todo cuando se produce la próxima temporada de transmisión. Así, en el mayor plazo posible de tiempo, se tiende a mantener un gran número de personas susceptibles entre la misma población a pesar de los anteriores brotes, puesto que hay cuatro diferentes cepas del virus del dengue y porque nuevos individuos son susceptibles de entrar en la población, ya sea a través de la inmigración o el parto.
El dengue posee una extensión geográfica similar a la de la malaria (en países tropicales y subtropicales) pero a diferencia de esta, el dengue se encuentra en zonas urbanas.
Cada serotipo es bastante diferente, por lo que no existe protección y pueden ocurrir epidemias causadas por serotipos diferentes.
El dengue se transmite a los humanos por el mosquito Aedes aegypti, el cual es el principal vector de la enfermedad en el hemisferio occidental, aunque también es transmitido por el Aedes albopictus.
No es posible el contagio directo de una persona a otra.[16][17]
Se cree que los casos notificados son una representación insuficiente de todos los casos de dengue que existen, puesto que se ignoran los casos subclínicos y los casos en que el paciente no se presenta para recibir tratamiento médico. Con un tratamiento médico adecuado la tasa de mortalidad por dengue puede reducirse a menos de 1 en 1000.[18]
Durante los años 2000, en Sudamérica se ha registrado el más dramático incremento de la incidencia del dengue, especialmente en Brasil, Colombia, Ecuador, Paraguay, Perú y Venezuela.[19]
Actualmente, en Venezuela se produce aproximadamente el 70 % de todos los casos en América, mientras que Colombia es donde se ha registrado el mayor número de casos de dengue hemorrágico y de casos fatales en los últimos años.[19]
En Chile, el principal mosquito vector se encuentra solo en la Isla de Pascua, y todas las personas con dengue reportadas en ese país desde 2004 se habían infectado fuera de Chile.[17]
Otro país afectado por esta enfermedad es México. Los primeros reportes de dengue se registraron en 1941, cuando se notificaron 6955 casos en toda la república. Posteriormente se reportaron pocos casos, hasta su desaparición en 1963 gracias a la campaña de erradicación del mosquito Aedes, que mantuvo el dengue ausente durante 12 años. Sin embargo, en 1978 se reintrodujo en México, donde aumentaron los casos a partir de 1980, lo que convirtió el dengue en uno de los problemas actuales más importantes de salud pública a nivel nacional. A partir de su reintroducción, el dengue ha causado cuatro brotes epidémicos: el primero en 1980, en el cual se reportaron 51 406 casos y se detectó la circulación de DENV-1; el segundo en 1997, con 53 541 casos, de los cuales 980 correspondieron a FHD, y donde se observó la circulación predominante de DENV-3; el tercero en 2007, con 52 369 casos, 9433 de los cuales correspondieron a FHD, y el cuarto en 2009, con 55 961 casos, de los cuales 11 396 correspondieron a FHD. En los brotes de 2007 y 2009 se observó la circulación predominante de DENV-1 y 2[20]

Hay pruebas importantes, originalmente sugeridas por S. B. Halstead en los años setenta, en las que es más probable que el dengue hemorrágico ocurra en pacientes que presentan infecciones secundarias por serotipos diferentes a la infección primaria. Un modelo para explicar este proceso ―que se conoce como anticuerpo dependiente de la mejora (ADM)― permite el aumento de la captación y reproducción de los viriones durante una infección secundaria con una cepa diferente. A través de un fenómeno inmunitario conocido como el pecado original antigénico, el sistema inmunitario no es capaz de responder adecuadamente a la fuerte infección, y la infección secundaria se convierte en mucho más grave.[21] Este proceso también se conoce como superinfección.[22]
En 2017 se informó una reducción significativa en América, de 2 177 171 casos en 2016 a 584 263 casos en 2017. Esto representa una reducción del 73 %. Durante 2017, Panamá, Perú y Aruba fueron los únicos países que registraron un aumento de casos. De manera similar, también se registró una reducción del 53 % en los casos de dengue grave. Justo durante el período posterior al brote de Zika (después de 2016) se registró una disminución de los casos de dengue y aún se desconocen los factores exactos que llevaron a esta disminución.[23]
En 2019 se registró la mayor cantidad de casos de dengue notificados a nivel mundial. Pasó de 0.5054 millones de casos (en 2000) a más de 2.4 millones (en 2010) y 5.2 millones (en 2019). Todas las regiones de la OMS se vieron afectadas y se registró por primera vez la transmisión del dengue en Afganistán.[23]
La pandemia de covid-19 ejerció una enorme presión sobre los sistemas de atención y gestión de la salud en todo el mundo. La OMS enfatizó la importancia de mantener los esfuerzos para prevenir, detectar y tratar enfermedades transmitidas por vectores como el dengue y otras enfermedades arbovirales durante aquel período crucial, ya que el número de casos aumentó en varios países, lo que expuso a las poblaciones urbanas con mayor riesgo de contraer ambas enfermedades. El impacto combinado de covid-19 y las epidemias de dengue puede potencialmente tener consecuencias devastadoras para las poblaciones en riesgo.[24]
En 2023 volvieron a surgir nuevos brotes de dengue a lo largo del planeta. En América Latina, desde principios de 2023, se han registrado brotes de dengue de magnitud considerable en la región de las Américas de la OMS, y se han notificado cerca de tres millones de casos sospechosos y confirmados de dengue en lo que va de año, cifra que supera los 2,8 millones de casos registrados a lo largo de 2022.
En Bangladés (Asia), del 1 de enero al 7 de agosto de 2023, el Ministerio de Salud y Bienestar de la Familia notificó un total de 69 483 casos de dengue y 327 muertes conexas, lo que supone una tasa de letalidad del 0,47 %. Aunque el dengue es endémico en Bangladés, el importante incremento de la enfermedad, que comenzó alrededor de finales de junio de 2023, no es habitual ni para la época del año ni si se compara con años anteriores.
En Chad (África), el 15 de agosto de 2023, el Ministerio de Salud Pública y Prevención declaró un brote de dengue. Al 1 de octubre, se habían registrado 1342 presuntos casos, así como 41 casos confirmados notificados en ocho distritos de salud en cuatro provincias. Entre los casos confirmados se notificó una muerte. Dadas las condiciones ambientales favorables para la propagación de los mosquitos, la crisis humanitaria en curso debido a la afluencia masiva de refugiados y repatriados de la tercera guerra civil sudanesa y la capacidad limitada de respuesta, la OMS considera que el riesgo que plantea este brote a nivel nacional es alto.[25][26][27]
Etiología[editar]
| Virus del dengue | ||
|---|---|---|
 Micrografía de microscopio electrónico mostrando el virus causante de la fiebre hemorrágica del dengue | ||
| Taxonomía | ||
| Familia: | Flaviviridae | |
| Género: | Flavivirus | |
| Clasificación de Baltimore | ||
| Grupo: | IV (Virus ARN monocatenario positivo) | |
| Especies | ||
| ||
El dengue es producido por un virus del grupo de los arbovirus (llamados así porque son transmitidos a través de artrópodos hematófagos), familia de los Flaviviridae, género Flavivirus. La partícula viral tiene forma esférica y mide entre 30 y 50 nm. Posee una envoltura proteica (principalmente E y M) que la cubre por completo. El material genético se encuentra contenido en un nucleocápside circular, y entre este y la cubierta se encuentra una bicapa lipídica que es formada a partir de lípidos extraídos de la membrana celular de la célula huésped. El genoma se compone de una sola cadena de ARN de tipo lineal, sentido positivo y gran variabilidad. El virus es altamente inestable en el medio ambiente, inactivándose con el calor, desecación y desinfectantes que contengan detergentes o solventes lipídicos.
Existen 5 serotipos de virus Dengue: DEN_1, DEN_2, DEN_3 y DEN_4. El DEN_5 serotipo fue descubierto en octubre del 2013, este serotipo sigue el ciclo selvático a diferencia de los otros cuatro serotipos que siguen el ciclo humano.[28] Cada uno de ellos crea inmunidad específica para toda la vida para reinfección por el mismo serotipo, así como inmunidad cruzada de corto plazo (algunos meses) para los otros 3 serotipos. Los cuatro serotipos pueden causar cuadros asintomáticos, febriles o mortales. Se han detectado algunas variables genéticas dentro de cada serotipo que parecen ser más virulentas o tener mayor potencial epidémico que otras.
Virología[editar]
Cualquiera de los cuatro tipos del virus es capaz de producir el dengue clásico. Se plantea que una infección inicial crea las condiciones inmunológicas para que una infección subsecuente produzca un dengue hemorrágico; sin embargo, otros plantean que una primera infección por dengue sea capaz de producir de una vez un dengue hemorrágico.[29]
Los serotipos 1 y 2 fueron aislados en 1945, y en 1956 los tipos 3 y 4; siendo el virus tipo 2 el más inmunogénico de los cuatro.[29]
El virus del dengue, al igual que otros flavivirus, contiene un genoma de ARN rodeado por una nucleocápside de simetría icosaédrica, de 30 nm de diámetro, la cual está constituida por la proteína C ―de 11 kd― y una envoltura lipídica de 10 nm de grosor asociadas a una proteína de membrana (M) y otra de envoltura (E), que da lugar a las proyecciones que sobresalen de la superficie de los viriones.[30]
Transmisión[editar]


El vector principal del dengue es el mosquito Aedes aegypti. El virus se transmite a los seres humanos por la picadura de mosquitos hembra infectadas. Tras un periodo de incubación del virus que dura entre 4 y 10 días, un mosquito infectado puede transmitir el agente patógeno durante toda su vida.[4] También es un vector el Aedes albopictus, este es un vector secundario cuyo hábitat es Asia, aunque debido al comercio de neumáticos se ha extendido en los últimos años a América y Europa. Tiene una gran capacidad de adaptación, y gracias a ello puede sobrevivir en las temperaturas más frías de Europa, lo cual es un grave problema de salud pública. Su tolerancia a las temperaturas bajo cero, su capacidad de hibernación y su habilidad para guarecerse en microhábitats son factores que propician su propagación y la extensión geográfica del dengue.[31]
Las personas infectadas son los portadores y multiplicadores principales del virus, y los mosquitos se infectan al picarlas. Tras la aparición de los primeros síntomas, las personas infectadas con el virus pueden transmitir la infección (durante 4 o 5 días; 12 días como máximo) a los mosquitos Aedes.[4]
El Aedes aegypti es una especie principalmente diurna, con mayor actividad a media mañana y poco antes de oscurecer. Vive y deposita sus huevos en el agua, donde se desarrollan sus larvas; a menudo en los alrededores o en el interior de las casas, tanto en recipientes expresamente utilizados para el almacenamiento de agua para las necesidades domésticas como en jarrones, tarros, neumáticos viejos y otros objetos que puedan retener agua estancada. Habitualmente no se desplazan a más de 100 m, aunque si la hembra no encuentra un lugar adecuado de ovoposición puede volar hasta 3 km, por lo que se suele afirmar que el mosquito que pica es el mismo que uno ha «criado». Solo pican las hembras, los machos se alimentan de savia de las plantas y no son vectores. La persona que es picada por un mosquito infectado puede desarrollar la enfermedad, que posiblemente es peor en los niños que en los adultos. La infección genera inmunidad de larga duración contra el serotipo específico del virus. No protege contra otros serotipos y, posteriormente, esto es lo que puede dar lugar a la forma de dengue hemorrágico.
El dengue también se puede transmitir por vía sanguínea, es decir, por productos sanguíneos contaminados y por donación de órganos.[32][33] En algunos países como Singapur, donde el dengue es endémico, el riesgo estimado de transmisión por transfusiones sanguíneas está entre 1,6 y 6 por cada 10 000 transfusiones.[34] La transmisión vertical (de madre a hijo) durante la gestación o en el parto han sido descritas.[35] También se ha dado un caso de transmisión sexual entre hombres.[36]
Predisposición[editar]
Se han descrito polimorfismos (variaciones genéticas que afectan al menos al 1 % de la población) asociados a un incremento del riesgo de padecer un dengue grave o complicaciones graves del dengue. Los ejemplos incluyen los genes que codifican para la proteína conocida como TNFα,[15] o también para las proteínas TGF-β, CTLA-4, DC-SIGN, PLCE1, y particulares formas alélicas de los complejos mayores de histocompatibilidad MHC humanos. Una anomalía genética común en la población africana, conocida como deficiencia de glucosa-6-fosfato, parece aumentar el riesgo de padecer formas graves y hemorrágicas de dengue.[37] Los polimorfismos en los genes del receptor de vitamina D y del receptor FcγR de las gammaglobulinas, que se han descrito parecen ofrecer cierta protección contra el desarrollo las formas graves del dengue, tras la infección con un segundo serotipo.
Patogenia[editar]
Cuando un mosquito infectado que lleva el virus del dengue pica a una persona, el virus entra en la piel junto con la saliva del mosquito.[37] El virus se une y entra en los macrófagos, donde se reproduce mientras los macrófagos viajan por todo el cuerpo.[37] Los macrófagos responden produciendo proteínas de señalización e inflamación para activar al sistema inmune, como citoquinas e interferón, los cuales van a ser responsables de los síntomas, como la fiebre, los dolores y los demás síntomas gripales. Como vemos, el virus no es directamente el agente lesivo, sino que los síntomas son debidos a la respuesta inmune del organismo.[37] En las formas graves, la producción del virus en el interior del organismo es enorme, y otros órganos pueden verse afectados, como el hígado o la médula ósea. Normalmente, las formas graves aparecen cuando existe una segunda exposición a un serotipo diferente del dengue del de la primera exposición. De esta manera, el sistema inmune está sensibilizado y responde de una forma más agresiva, generando peores síntomas.[37] Además, en estas formas graves se suele producir una disfunción endotelial, responsable de las hemorragias (cuadro más severo del dengue).[37]
Replicación viral[editar]
Una vez en la piel, el virus del dengue es reconocido y captado por las células de Langerhans (una subpoblación de células dendríticas) presentes en la piel que identifican patógenos.[37] El virus gracias a un receptor de endocitosis entra en la célula; esto se produce por la interacción entre proteínas virales de superficie y proteínas de membrana de la célula de Langerhans, especialmente una lectina tipo C llamada DC-SIGN, un receptor de manosa y la proteína CLEC5A. Se ha demostrado que el DC-SIGN, un receptor no específico de material extraño de las células dendríticas, es el punto principal que permite la entrada del virus al interior de la célula presentadora de antígenos. La célula de Langerhans migra hacia el ganglio linfático más cercano. Mientras tanto, en este recorrido, el genoma del virus es trasladado, en el interior de vesículas de membrana, hacia el retículo endoplasmático, donde se producen nuevas proteínas virales a través de la lectura del ARN viral, para comenzar a formar nuevos viriones. Las partículas inmaduras del virus son transportadas al aparato de Golgi, ya que ciertas proteínas del virus necesitan ser glicosiladas, es decir, necesitan añadir a sus cadenas moléculas glucídicas para ser estables. Esta glicosilación tiene lugar en el Golgi. Ahora estas proteínas se van a ensamblar, y van a viajar hacia la membrana de la célula de Langerhans, para salir al exterior mediante exocitosis. Ya están capacitados estos nuevos viriones para infectar a otras células blancas sanguíneas, como monocitos y macrófagos.
Formas graves[editar]
No está del todo claro por qué la infección secundaria con una cepa o serotipo diferente del virus del dengue produce un mayor riesgo de padecer dengue hemorrágico o síndrome del choque del dengue. La hipótesis más aceptada por la comunidad científica es la de la mejora dependiente de anticuerpos. El mecanismo exacto que está detrás no está del todo claro. Podría ser causado por la unión deficiente de anticuerpos no neutralizantes y la entrega en el compartimento equivocado de las células blancas de la sangre que han ingerido el virus para su destrucción. Recientemente, hay una gran sospecha de que la mejora dependiente de anticuerpos no es el único mecanismo que subyace al dengue grave, y sus complicaciones relacionadas.[15] Y, varias líneas de investigación actuales, han implicado a las células T y factores solubles tales como citocinas y sistema del complemento en la patogenia de estas formas graves.[37]
La enfermedad grave se caracteriza por los problemas en la permeabilidad capilar (disfunción capilar), una parte del líquido y algunas proteínas de la sangre se extravasan hacia el tejido extracelular debido a un aumento de la permeabilidad capilar; y además suceden en la sangre problemas de coagulación. Estos cambios por la infección vírica, aparecen asociados a un estado desordenado del glicocálix endotelial, que actúa como un filtro para los componentes sanguíneos. Este desorden se cree que está causado por la respuesta immune frente al virus. Otros procesos de interés que ocurren en estas formas graves del dengue incluyen a células infectadas que se vuelven necróticas, y a plaquetas y factores de la coagulación, que también intervienen en este caos hemodinámico.[37]
Cuadro clínico[editar]
El cuadro clínico de la fiebre dengue y la presentación de las diversas manifestaciones y complicaciones, varía de un paciente a otro. Típicamente, los individuos infectados por el virus del dengue son asintomáticos (80 %). Después de un período de incubación de entre cuatro y diez días, aparece un cuadro viral caracterizado por fiebre de más de 38 °C, dolores de cabeza, dolor retroocular y dolor intenso en las articulaciones (artralgia) y músculos (mialgia) ―por eso se le ha llamado «fiebre rompehuesos»―, inflamación de los ganglios linfáticos y erupciones en la piel puntiformes de color rojo brillante, llamada petequia, que suelen aparecer en las extremidades inferiores y el tórax de los pacientes, desde donde se extiende para abarcar la mayor parte del cuerpo.[15][38]
Otras manifestaciones menos frecuentes incluyen:

- Trombocitopenia, disminución de la cuenta de plaquetas
- Hemorragias de orificios naturales: orina con sangre, hemorragia transvaginal
- Hemorragia de nariz
- Gingivitis y/o hemorragia de encías
- Gastritis, con una combinación de dolor abdominal
- Estreñimiento
- Complicaciones renales: nefritis
- Complicaciones hepáticas: hepatitis reactiva, Ictericia
- Inflamación del bazo
- Náuseas
- Vómitos
- Diarrea
- Percepción distorsionada del sabor de los alimentos (disgeusia)
Algunos casos desarrollan síntomas mucho más leves que pueden, cuando no se presente la erupción, ser diagnosticados como resfriado, estas formas leves, casi subclínicas, aparecen generalmente con la primera infección (solo ha habido contacto con un serotipo). Así, los turistas de las zonas tropicales pueden transmitir el dengue en sus países de origen, al no haber sido correctamente diagnosticados en el apogeo de su enfermedad. Los pacientes con dengue pueden transmitir la infección solo a través de mosquitos o productos derivados de la sangre y solo mientras se encuentren todavía febriles; por eso, es raro que existan epidemias de dengue fuera del área geográfica del vector.[15]
Los signos de alarma en un paciente con dengue que pueden significar un colapso circulatorio inminente incluyen:[39]
- Estado de choque
- Distensión y dolor abdominal
- Frialdad en manos y pies con palidez exagerada
- Sudoración profusa y piel pegajosa en el resto del cuerpo
- Hemorragia por las mucosas, como encías o nariz
- Somnolencia o irritabilidad
- Taquicardia, hipotensión arterial o taquipnea
- Dificultad para respirar
- Convulsiones
Complicaciones[editar]
El dengue ocasionalmente puede afectar a varios órganos diferentes. Genera un descenso del nivel de conciencia en un 0.5-6 % de los afectados, lo cual es atribuido a una encefalitis (infección del cerebro por parte del virus) o indirectamente como resultado de la afectación de otros órganos, por ejemplo, del hígado, en una encefalopatía hepática.[11] Otros desórdenes neurológicos han sido descritos en el contexto de una fiebre por dengue, como un Síndrome de Guillain-Barré.
Diagnóstico[editar]
Desde finales de 2008 la definición de dengue cambió, debido a que la antigua clasificación de la OMS era muy rígida y los criterios que utilizaban para la definición de caso de fiebre del dengue hemorrágico requerían la realización de exámenes de laboratorio que no estaban disponibles en todos los lugares, si bien la prueba de torniquete se usó y sigue usándose en lugares que adolecen de falta de medios más precisos. Por esta razón hasta en el 40 % de los casos no era posible aplicar la clasificación propuesta. Adicionalmente entre el 15 y el 22 % de los pacientes con choque por dengue no cumplían los criterios de la guía, por lo cual no se les daba un tratamiento oportuno. Tras varios esfuerzos de grupos de expertos en Asia y América, la realización de varios estudios, como el DENCO (Dengue Control), la clasificación cambió a dengue y dengue grave. Esta clasificación es más dinámica y amplia, permitiendo un abordaje más holístico de la enfermedad.[40][41]
La enfermedad ―a pesar de ser una sola―[42] tiene dos formas de presentación: dengue y dengue grave. Después de un periodo de incubación de 2 a 8 días, en el que puede parecer un cuadro catarral sin fiebre, la forma típica se expresa con los síntomas anteriormente mencionados. Hasta en el 80 % de los casos la enfermedad puede ser asintomática o leve, incluso pasando desapercibida. La historia natural de la enfermedad describe típicamente tres fases clínicas: Una fase febril, que tiene una duración de 2 a 7 días, una fase crítica, donde aparecen los signos de alarma de la enfermedad (dolor abdominal, vómito, sangrado de mucosas, alteración del estado de conciencia), trombocitopenia, las manifestaciones de daño de órgano (hepatopatías, miocarditis, encefalopatía, etc.), el choque por extravasación de plasma o el sangrado severo (normalmente asociado a hemorragias de vías digestivas). Finalmente, está la fase de recuperación, en la cual hay una elevación del recuento plaquetario y de linfocitos, estabilización hemodinámica, entre otros.[43]
La definición de caso probable de dengue, tiene los siguientes criterios:[44] Un cuadro de fiebre de hasta 7 días, de origen no aparente, asociado a la presencia de dos o más de los siguientes:
- Cefalea (dolor de cabeza)
- Dolor retroocular (detrás de los ojos)
- Mialgias (dolor en los músculos)
- Artralgias (dolor en las articulación)
- Postración
- Exantema
- Puede o no estar acompañado de hemorragias
- Antecedente de desplazamiento (hasta 15 días antes del inicio de síntomas) o que resida en un área endémica de dengue
La definición de dengue grave:[44]
- Extravasación de plasma que conduce a: choque o acumulación de líquidos (edema) con dificultad respiratoria
- Hemorragias severas
- Afectación severa de un órgano (hígado, corazón, cerebro)
- Trombocitopenia por debajo de 30 000
El diagnóstico de laboratorio se puede realizar por distintas formas, que se agrupan en métodos directos e indirectos.[45]
- Métodos directos
- Aislamiento viral: se realiza con una prueba en el suero durante las primeras 72 horas.
- RCP: detección del ácido nucleico
- NS1: detección de la proteína no estructural 1 (NS1) en suero
- Métodos indirectos
- IgM dengue: detección de anticuerpo en sangre. Se realiza en sangre después del quinto día de la enfermedad.
- Otros hallazgos de laboratorio
- Leucopenia
- Trombocitopenia
- Hipoalbuminemia
- Hemoconcentración con aumento del hematocrito. Este último hallazgo es secundario a la extravasación de plasma que sufren los pacientes, en donde también se puede encontrar ascitis y derrame pleural.
Diagnóstico diferencial[editar]
El diagnóstico diferencial incluye todas las enfermedades epidemiológicamente importantes incluidas bajo los rubros de fiebres víricas transmitidas por artrópodos, sarampión, rubéola, y otras enfermedades febriles sistémicas, además de la malaria, leptospirosis, fiebre tifoidea y meningococcemia. Como técnicas auxiliares en el diagnóstico pueden utilizarse las pruebas de inhibición de la hemaglutinación, fijación del complemento, ELISA, captación de anticuerpos IgG e IgM, así como las de neutralización. El virus se aísla de la sangre por inoculación de mosquitos o por técnicas de cultivo celular de mosquitos.
Tratamiento[editar]
A pesar de que no existía un medicamento específico para tratar esta enfermedad, actualmente sí existe un tratamiento basado en las manifestaciones clínicas que han demostrado reducir la mortalidad. Las nuevas guías de la OMS establecen tres grupos terapéuticos:
- Grupo A: pacientes que pueden ser enviados a su casa porque no tienen alteración hemodinámica, no pertenecen a un grupo de riesgo ni tienen signos de alarma. El manejo se basa en el aumento de la ingesta de líquidos orales se recomienda para prevenir la deshidratación. Para aliviar el dolor y la fiebre es muy importante evitar la aspirina y los fármacos antiinflamatorios no esteroides, ya que estos medicamentos pueden agravar la hemorragia asociada con algunas de estas infecciones, por sus efectos anticoagulantes,[46] en su lugar los pacientes deben tomar acetaminofén para el manejo de la fiebre y el dolor de cabeza
- Grupo B: pacientes con signos de alarma y/o que pertenecen a un grupo de riesgo. Dichos pacientes requieren hospitalización por al menos 72 horas para hacer reposición de líquidos endovenosos, monitoreo estricto de signos vitales, gasto urinario y medición de hematocrito.
- Grupo C: pacientes con diagnóstico de dengue grave, que requieren manejo en Unidades de Cuidado Intensivo.[47]
La búsqueda de tratamientos específicos para la enfermedad ha llevado a académicos a realizar estudios para reducir la replicación del virus, que está relacionada con la gravedad de las manifestaciones clínicas. Existen varios ensayos clínicos en donde se tiene en cuenta la fisiopatología de la enfermedad, que sugiere que los cuadros clínicos graves tienen el antecedente de exposición al virus, que genera una memoria inmunológica. Esta memoria al tener contacto con el virus en una segunda exposición desencadena una respuesta exagerada del sistema inmunológico. Teniendo en cuenta esta explicación de la fisiopatología, se sugiere que medicamentos moduladores de la respuesta inmunitaria como esteroides, cloroquina, ácido micofenólico y la ribavirina inhiben la replicación del virus.[48] Sin embargo, estos estudios no son concluyentes y no se recomienda su uso actualmente.
Medidas preventivas y profilaxis[editar]

- Específica: En diciembre de 2015 se anunció la conclusión de la vacuna tetravalente, eficaz para la prevención del dengue en personas mayores de 9 y hasta 45 años.[49] La vacuna Dengvaxia de laboratorios Sanofi Pasteur ha sido aprobada para su uso en varios países endémicos para esta enfermedad.[50] El uso de esta vacuna solo se recomienda para aquellos individuos que han sufrido previamente una infección por alguno de los serotipos que causan la enfermedad.[51][52]
- Inespecífica:
- Utilizar repelentes adecuados, los recomendados son aquellos que contengan DEET (dietiltoluamida) en concentraciones del 30 al 35 % y deben aplicarse durante el día en las zonas de la piel no cubiertas por la ropa.
- Evitar el uso de perfumes, evitar el uso de ropas de colores oscuros.
- La ropa debe ser impregnada con un repelente que contenga permetrina (antipolillas para ropa y telas) la cual mantiene el efecto por 2 a 3 meses a pesar de 3 a 4 lavados.
- Evitar que los mosquitos piquen al enfermo y queden infectados, colocando un mosquitero en su habitación (preferiblemente impregnado con insecticida) hasta que ya no tenga fiebre.
- Buscar en el domicilio posibles criaderos de mosquitos y destruirlos. En los recipientes capaces de contener agua quieta, generalmente de lluvia, es donde comúnmente se cría el mosquito: recipientes abiertos, llantas, coladeras.
- Estos criaderos se deben eliminar: colocando tapaderas bien ajustadas en los depósitos de agua para evitar que los mosquitos pongan allí sus huevos. Si las tapaderas no ajustan bien, el mosquito podrá entrar y salir.
- Se deben tapar fosas sépticas y pozos negros, obturando bien la junta a fin de que los mosquitos del dengue no puedan establecer criaderos.
- En las basuras y los desechos abandonados en torno a las viviendas se puede acumular el agua de lluvia. Conviene pues desechar ese material o triturarlo para enterrarlo luego o quemarlo, siempre que esté permitido.
- Limpiar periódicamente los canales de desagüe.[53]
Típicamente, las medidas preventivas deben abarcar estas áreas:
- Realización de encuestas epidemiológicas y de control larvario. Encuestas en la localidad para precisar la densidad de la población de mosquitos vectores, identificar sus criaderos (respecto a Aedes aegypti por lo común comprende recipientes naturales o artificiales en los que se deposita por largo tiempo en agua limpia, cerca o dentro de las viviendas, por ejemplo, neumáticos viejos y otros objetos). Los neumáticos en desuso con agua, los tanques, floreros de cementerio, macetas, son algunos de los hábitats más comunes de los mosquitos del dengue.
- Promoción de conductas preventivas por parte de la población.
- - Educación sobre el dengue y su prevención. Riesgo, susceptibilidad y severidad del dengue, incluido el hemorrágico. Descripción del vector, horarios de actividad, radio de acción, etc. Descripción de las medidas preventivas.
- - Eliminación de criaderos de larvas. Limpiar patios y techos de cualquier potencial criadero de larvas. Para los tanques se recomienda agregar pequeñas cantidades de cloro sobre el nivel del agua. Para los neumáticos simplemente vacíelos. Puede colocarle arena para evitar la acumulación de líquido. Otra solución es poner peces guppy (Poecilia reticulata) en el agua, que se comerán las larvas.
- - Utilización de barreras físicas (utilización de mosquiteros en ventanas, telas al dormir).
- - Utilización de repelentes de insectos. Especificar cuáles y cómo deben usarse.
- Eliminación de criaderos de larvas por el mismo sector público. Debido a la falta de éxito en la adopción de estas conductas, usualmente el sector público termina realizándolas.
- Comunicación de riesgos a través de medios masivos. Es imprescindible aumentar el riesgo percibido, la susceptibilidad percibida y el valor percibido de las medidas precautorias por parte de la población para que esta las adopte.
Controles sanitarios[editar]

- Notificación a la autoridad local de salud. Notificación obligatoria de las epidemias, pero no de los casos individuales, clase 4.
- Aislamiento. Precauciones pertinentes para la sangre. Evitar el acceso de los mosquitos de actividad diurna a los pacientes, hasta que ceda la fiebre, colocando una tela metálica o un mosquitero en las ventanas y puertas de la alcoba del enfermo, un pabellón de gasa alrededor de la cama del enfermo o rociando los alojamientos con algún insecticida que sea activo contra las formas adultas o que tenga acción residual, o colocando un mosquitero alrededor de la cama, de preferencia impregnando con insecticida.
- Desinfección concurrente.
- Cuarentena.
- Inmunización de contactos. Si el dengue surge cerca de posibles focos selváticos de fiebre amarilla, habrá que inmunizar a la población contra esta última, porque el vector urbano de las dos enfermedades es el mismo.
- Investigación de los contactos y de la fuente de infección. Identificación del sitio de residencia del paciente durante la quincena anterior al comienzo de la enfermedad, y búsqueda de casos no notificados o no diagnosticados.
Brotes[editar]
En 2008[editar]
El 20 de marzo de 2008, el secretario de salud del estado de Río de Janeiro, Sérgio Côrtes, anunció que 23 555 casos de dengue, incluyendo 30 muertes, se han registrado en el estado en menos de tres meses. Côrtes dijo, «Estoy tratando esto como una epidemia debido a que el número de casos es muy elevado». El ministro federal de salud del estado, José Gomes Temporão, también anunció que estaba formando una brigada para responder a la situación. Cesar Maia, alcalde de la ciudad de Río de Janeiro, negó que exista un grave motivo de preocupación, diciendo que la incidencia de casos fue, de hecho, la disminución de su punto máximo a principios de febrero.[54] El 3 de abril de 2008, el número de casos notificados aumentó a 55.000[55] Para finales de marzo de 2008 la OMS había reportado 120 570 casos de dengue y dengue hemorrágico en Brasil, siendo el serotipo principal el DEN-3.[56]
En 2009[editar]
Santa Cruz de la Sierra (Bolivia), empezó una epidemia de dengue a principios de 2009, con casos esporádicos en el resto del país. Esta epidemia ha afectado a la fecha (31 de enero de 2009) a más de 50 000 personas y producido la muerte a cinco, por casos de dengue hemorrágico. Hasta el 19 de febrero de 2009 se han reportado 15 816 casos de dengue en Bolivia, distribuidos en las ciudades de Santa Cruz, Trinidad, Riberalta, Tarija y Guayaramerín; con 64 casos de dengue hemorrágico y seis personas fallecidas (incluido un niño proveniente de la zona de Los Yungas, en La Paz).
En Salvador Mazza, provincia de Salta, Argentina, localidad fronteriza que limita con Bolivia, en febrero de 2009 se presentaron numerosos casos de dengue, detectados en niños y adultos. A esta fecha (abril de 2009) se conoce un caso de muerte de un menor por el dengue hemorrágico.[57]
En Charata, Provincia del Chaco, Argentina, desde febrero de 2009, al igual que casi toda la provincia, comienza una epidemia que al 31 de marzo tiene dos muertes, y una cantidad aproximada de 2500 casos oficialmente declarados en la región. Alarmantemente los números siguieron creciendo. Al 10 de abril de 2009 la cantidad de infectados ascendía a 14 500.
Un trabajo en 2009 del ingeniero agrónomo Alberto Lapolla[58] vincula la epidemia de dengue con la sojización. En su estudio se señala la equivalencia del mapa de la invasión de mosquitos portadores del mal del dengue con el de Bolivia, Paraguay, Argentina, Brasil y Uruguay, donde el poroto de soja transgénico de Monsanto se fumiga con el herbicida glifosato, y con 2-4-D, atrazina, endosulfán, paraquat, diquat y clorpirifós. Todos estos venenos matan peces y anfibios, sapos, ranas, etc., los predadores naturales de los mosquitos, de los que se alimentan tanto en su estado larval como de adultos. Esto se comprueba en la casi desaparición de la población de anfibios en la pradera pampeana y en sus cursos de agua principales, ríos, arroyos, lagunas, así como el elevado número de peces que aparecen muertos o con deformaciones físicas y afectados en su capacidad reproductiva. A esto debe sumarse la deforestación en las áreas boscosas y de monte del Noreste y el Noroeste argentino, que destruyó su equilibrio ambiental, liquidando el refugio y hábitat natural de otros predadores de los mosquitos, lo cual permite el aumento descontrolado de su población.
En Perú también se encuentra presente el dengue, en las zonas de Piura, Sullana, Talara, Jaén, Amazonas, Loreto, Bagua y en Utcubamba.
En 2013[editar]
La epidemia de dengue en Paraguay fue un brote epidémico de dengue en Paraguay ocurrido ya desde finales del año 2012 y durante todo el año 2013 prácticamente, siendo el peor registrado en la historia del país hasta la del 2019-2020 pero siendo aun así la más mortal.
Según las cifras del Dirección de Vigilancia de la Salud y del propio Ministerio de Salud de Paraguay, se confirmaron más de 130 mil casos de unos 150mil casos posibles (sospechosos), y 252 fallecieron, en un país de sólo 6,7 millones de habitantes.[59] En Asunción y Central se registraron alrededor del 80% del total de los casos confirmados de dengue.[60]En 2016[editar]
Brote Dengue Autóctono en Uruguay, Argentina y España[61] de febrero de 2016,[62] el primero se registró el 15 de febrero de 2016. Al 23 de febrero ya son nueve los casos autóctonos siendo uno de ellos grave. Por primera vez en muchos años se detectaron casos autóctonos de Dengue en Uruguay, siete en la capital Montevideo en los Barrios de Pocitos, Malvín Norte y La Unión[63] y los otros dos casos en los departamentos de Salto y San José respectivamente.[64]
En 2019 y 2021[editar]

La epidemia de dengue de 2019-2021 fue una epidemia de la enfermedad del dengue, causada por el virus del dengue (DEN) y transmitida por los mosquitos del género Aedes, en particular la especie Aedes aegypti, que ha provocado una epidemia en varios países del mundo, afectando principalmente al Sudeste Asiático y Latinoamérica.[65][66] Entre los países con mayor cantidad de enfermos y muertes se incluyen, en la región asiática, Filipinas, Vietnam, Malasia, Bangladés, Tailandia, Camboya, Laos y Singapur, mientras que en América se registró principalmente en Brasil, México, Colombia, Nicaragua, Paraguay, Bolivia y la mayor parte de Centroamérica.[67]
La propagación de la enfermedad ha aumentado en aquellas áreas donde han disminuido los niveles de vacunación, donde no se realizan las medidas de prevención adecuadas, y donde crece la población de mosquitos, que son los principales portadores de la enfermedad, y que pueden reproducirse en grandes cantidades especialmente en climas cálidos y húmedos.En 2024[editar]
Argentina sufrió la mayor epidemia de Dengue en su historia debido a que el Gobierno de Milei no se implementó en el calendario de vacunación.[68][69][70]
Incidencia del dengue en países tropicales[editar]
Perú[editar]
A continuación se presenta una tabla con la cantidad de casos registrados desde el año 2014 en el Perú:[71][72]
| Año | N° de casos | Fallecidos |
|---|---|---|
| 2014 | 17 234 | ID |
| 2015 | 35 816 | ID |
| 2016 | 26 433 | ID |
| 2017 | 68 290 | 89 |
| 2018 | 4698 | 18 |
| 2019 | 15 287 | 37 |
| 2020 | 47 932 | 86 |
| 2021 | 44 781 | 43 |
| 2022 | 63 211 | 81 |
| 2023 | 270 978 | 445 |
El brote de 2023, el cual fue agudizado por el paso del ciclón Yaku, es considerado el peor rebrote de dengue en el Perú. Entre las causas de esta expansión y el incremento se ha identificado el cambio climático, fenómeno el niño, deterioro de las condiciones de vida de mucha población.[72]
Medidas en caso de epidemia[editar]
Búsqueda y destrucción de especies de mosquitos en las viviendas y eliminación de los criaderos, aplicación de larvicida «Abate» (supresor del crecimiento de la larva en estado de pupa en agua) en todos los posibles sitios de proliferación de St. aegypti
Utilizar repelente de insectos (para que no ocurra el contagio). Además existen varios elementos de destrucción de larvas que producen el dengue como insecticidas o pesticidas.
Repercusiones en caso de desastre[editar]
Las epidemias pueden ser extensas, en especial como consecuencia de huracanes, tormentas tropicales o inundaciones.
Cuando estalla un brote epidémico de dengue en una colectividad o un municipio, es necesario recurrir a medidas de lucha antivectorial, en particular con el empleo de insecticidas por nebulización o por rociado de volúmenes mínimos del producto. De este modo se reduce el número de mosquitos adultos del dengue frenando la propagación de la epidemia. Durante la aspersión, los miembros de la comunidad deben cooperar dejando abierta las puertas y ventanas a fin de que el insecticida entre en las casas y maten a los mosquitos que se posan en su interior.
Imprescindible la eliminación de basura y chatarra y otras acumulaciones de agua estancada.
Medidas internacionales[editar]
Cumplimiento de los acuerdos internacionales destinados a evitar la propagación de Aedes aegypti por barcos, aviones o medios de transporte terrestre desde las zonas donde existe infestaciones.
Erradicación[editar]

Se ha observado que la bacteria Wolbachia reduce la sensibilidad de Aedes aegypti al virus del dengue, por lo que se ha propuesto introducirla en poblaciones salvajes de este insecto para reducir la población de mosquitos infectados.[73]
Un ensayo preliminar confirmó que mosquitos inoculados con Wolbachia y liberados al ambiente transmitieron la bacteria a la población local de Aedes aegypti, lo cual sugiere que el uso de Wolbachia podría disminuir drásticamente la incidencia de la enfermedad.[73]
Uso como arma biológica[editar]
El virus del dengue formó parte de una docena de agentes que los EE. UU. estudiaron como potenciales armas biológicas antes de suspender su programa de armas biológicas.[74]
Véase también[editar]
- Enfermedad infecciosa
- Fiebre amarilla
- Flavivirus
- Fiebre de Zika
- Arbovirus
- Enfermedades de origen hídrico
- Aedes aegypti
- Tifus murino
- Malaria
- Chikungunya
Referencias[editar]
- ↑ «Dengue and severe dengue». www.who.int (en inglés). Consultado el 21 de noviembre de 2022.
- ↑ CNN, Susie East, for. «World's first dengue fever vaccine launched». CNN. Consultado el 21 de noviembre de 2022.
- ↑ «Chapter 4, Prevention of Specific Infectious Diseases». CDC Traveler's Health: Yellow Book. Archivado desde el original el 21 de mayo de 2007. Consultado el 20 de mayo de 2007.
- ↑ a b c «http://www.who.int/mediacentre/factsheets/fs117/es/».
- ↑ Harapan, Harapan; Michie, Alice; Sasmono, R. Tedjo; Imrie, Allison (30 de julio de 2020). «Dengue: A Minireview». Viruses (en inglés) 12 (8): 829. ISSN 1999-4915. PMC 7472303. PMID 32751561. doi:10.3390/v12080829. Consultado el 20 de septiembre de 2021.
- ↑ a b «etymologia: dengue» (PDF). Emerging Infectious Diseases 12 (6): 893. 2006. Archivado desde el original el 28 de noviembre de 2007. Consultado el 26 de abril de 2009.
- ↑ a b Gubler DJ (julio de 1998). «Dengue and dengue hemorrhagic fever». Clinical microbiology reviews 11 (3): 480-96. PMC 88892. PMID 9665979. Consultado el 30 de abril de 2013.
- ↑ a b c d e Gubler, DJ (2006). «Dengue/dengue haemorrhagic fever: history and current status». Novartis Found Symp (en inglés) 277: 3-16. PMID 17319151. Consultado el 30 de abril de 2013.
- ↑ Gubler, DJ (febrero de 2002). «Epidemic dengue/dengue hemorrhagic fever as a public health, social and economic problem in the 21st century». TRENDS in microbiology (en inglés) 10 (2): 100-103. Archivado desde el original el 21 de octubre de 2012. Consultado el 30 de abril de 2013.
- ↑ a b c Henchal, EA; Putnak, JR (octubre de 1990). «The dengue viruses». Clin. Microbiol. Rev (en inglés) 3 (4): 376-96. PMC 358169. PMID 2224837. doi:10.1128/CMR.3.4.376. Archivado desde el original el 25 de julio de 2011. Consultado el 30 de abril de 2013.
- ↑ a b Gould EA, Solomon T (febrero de 2008). «Pathogenic flaviviruses». The Lancet 371 (9611): 500-9. PMID 18262042. doi:10.1016/S0140-6736(08)60238-X.
- ↑ «Dengue fever: essential data». 1999. Archivado desde el original el 11 de octubre de 2008. Consultado el 5 de octubre de 2008.
- ↑ Harper D (2001). «Etymology: dengue». Online Etymology Dictionary. Consultado el 5 de octubre de 2008.
- ↑ World Health Organization (noviembre de 2012). «Dengue and severe dengue». Consultado el 30 de abril de 2013.
- ↑ a b c d e Whitehorn J, Farrar J (2010). «Dengue». Br. Med. Bull. 95: 161-73. PMID 20616106. doi:10.1093/bmb/ldq019.
- ↑ Cartilla de información acerca de la fiebre del dengue, publicado en octubre de 2006 en el sitio web de la OMS. Consultado el 30 de noviembre de 2007.
- ↑ a b El Mercurio (26 de febrero de 2006). «Minsal confirma cuatro casos de dengue en Chile». Consultado el 21 de octubre de 2009.
- ↑ Bhatt nombre=S.; Gething, P.W.; Brady, O.J. (abril de 2013). «The global distribution and burden of dengue». Nature 496 (7446): 504-507. PMC 3651993. PMID 23563266. doi:10.1038/nature12060.
- ↑ a b Díaz Quijano, Freddy Alexander (2008): «Predictores de sangrado espontáneo en dengue: una revisión sistemática de la literatura», artículo publicado en marzo de 2008 en el sitio web de la revista Investigación Clínica [online], volumen 49, n.º 1, págs. 111-122; marzo de 2008. ISSN 0535-5133. Consultado el 21 de octubre de 2009.
- ↑ Ivonne Torres-Galicia, David Cortés-Poza y Ingeborg Becker, Dengue en México: análisis de dos décadas (2014). Material y métodos. p. 123 y 124. Consultado el 01/10/2020.
- ↑ Rothman AL (2004). «Dengue: defining protective versus pathologic immunity». J. Clin. Invest. 113 (7): 946-51. PMID 15057297. doi:10.1172/JCI200421512.
- ↑ Nowak y mayo de 1994; Levin y Pimentel 1981.
- ↑ a b «Dengue and severe dengue».
- ↑ Cardona‐Ospina, Jaime A.; Arteaga‐Livias, Kovy; Villamil‐Gómez, Wilmer E.; Pérez‐Díaz, Carlos E.; Katterine Bonilla‐Aldana, D.; Mondragon‐Cardona, Álvaro; Solarte‐Portilla, Marco; Martinez, Ernesto et al. (2021-01). «Dengue and COVID‐19, overlapping epidemics? An analysis from Colombia». Journal of Medical Virology (en inglés) 93 (1): 522-527. ISSN 0146-6615. PMC 7323437. PMID 32558962. doi:10.1002/jmv.26194. Consultado el 20 de septiembre de 2021.
- ↑ «Dengue – Región de las Américas». www.who.int. Consultado el 1 de diciembre de 2023.
- ↑ «Dengue - Bangladesh». www.who.int. Consultado el 1 de diciembre de 2023.
- ↑ «Dengue - Chad». www.who.int. Consultado el 1 de diciembre de 2023.
- ↑ Mustafa, M.S.; Rasotgi, V.; Jain, S.; Gupta, V. (2015-1). «Discovery of fifth serotype of dengue virus (DENV-5): A new public health dilemma in dengue control». Medical Journal, Armed Forces India 71 (1): 67-70. ISSN 0377-1237. PMC 4297835. PMID 25609867. doi:10.1016/j.mjafi.2014.09.011. Consultado el 15 de febrero de 2018.
- ↑ a b DOTRES MARTINEZ, Carlos et al. Dengue hemorrágico en el niño (artículo completo disponible en español). Cad. Saúde Pública [online]. 1987, vol.3, n.2 [cited 2009-10-21], pp. 158-180. ISSN 0102-311X. doi 10.1590/S0102-311X1987000200004.
- ↑ TIBAIRE MONTES, M. Actualización en dengue: Parte 1 (artículo completo disponible en español). Rev. Soc. Ven. Microbiol. [online]. ene. 2001, vol.21, no.1 [citado 21 octubre de 2009], p.39-45. ISSN 1315-2556.
- ↑ «http://www.cdc.gov/ncidod/dvbid/arbor/albopic_new.htm».
- ↑ Wilder-Smith A, Chen LH, Massad E, Wilson ME (enero de 2009). «Threat of dengue to blood safety in dengue-endemic countries». Emerg. Infect. Dis. 15 (1): 8-11. PMC 2660677. PMID 19116042. doi:10.3201/eid1501.071097. Archivado desde el original el 1 de mayo de 2009. Consultado el 5 de abril de 2013.
- ↑ Stramer SL, Hollinger FB, Katz LM, et al. (agosto de 2009). «Emerging infectious disease agents and their potential threat to transfusion safety». Transfusion. 49 Suppl 2: 1S-29S. PMID 19686562. doi:10.1111/j.1537-2995.2009.02279.x.
- ↑ Teo D, Ng LC, Lam S (abril de 2009). «Is dengue a threat to the blood supply?». Transfus Med 19 (2): 66-77. PMC 2713854. PMID 19392949. doi:10.1111/j.1365-3148.2009.00916.x.
- ↑ Wiwanitkit V (enero de 2010). «Unusual mode of transmission of dengue». Journal of Infection in Developing Countries 4 (1): 51-4. PMID 20130380.
- ↑ «Dengue Madrid: Detectacto el primer caso de transmisión sexual». La Vanguardia. 7 de noviembre de 2019. Consultado el 7 de noviembre de 2019.
- ↑ a b c d e f g h i Martina BE, Koraka P, Osterhaus AD (octubre de 2009). «Dengue virus pathogenesis: an integrated view». Clin. Microbiol. Rev. 22 (4): 564-81. PMC 2772360. PMID 19822889. doi:10.1128/CMR.00035-09. Archivado desde el original el 18 de mayo de 2011. Consultado el 5 de abril de 2013.
- ↑ Reiter P (11 de marzo de 2010). «Yellow fever and dengue: a threat to Europe?». Euro Surveill 15 (10): 19509. PMID 20403310.
- ↑ Kroeger, Axel (2001). No mas problemas de salud. Editorial Pax México. pp. 163-169. ISBN 968860559X.
- ↑ DENCO (Dengue Control): an EU-TDR-Wellcome supported multicentre clinical prospective study in 7 countries.
- ↑ «Dengue: guidelines for diagnosis, treatment, prevention and control» (pág. 10). Ginebra: Organización Mundial de la Salud, 2009.
- ↑ «Dengue», artículo de Eric MARTÍNEZ TORRES en Estud. Av., volumen 22, n.º 64. San Pablo (Brasil), diciembre de 2008.
- ↑ «Dengue: guidelines for diagnosis, treatment, prevention and control» (págs. 25 a 30). Ginebra: Organización Mundial de la Salud, 2009.
- ↑ a b «Dengue: guidelines for diagnosis, treatment, prevention and control» (págs. 10 a 14). Ginebra: Organización Mundial de la Salud, 2009.
- ↑ «Dengue: guidelines for diagnosis, treatment, prevention and control» (pág. 94). Ginebra: Organización Mundial de la Salud, 2009.
- ↑ Dengue y fiebre DH: información para la Salud General, Centro de Control de Enfermedades (Estados Unidos), 22 de octubre de 2007.
- ↑ «Malagón JN, Padilla JC, Rojas-Alvarez DP. Guía de atención Clínica Integral del paciente con Dengue. Infectio. 2011; 15(4):293-301.». Archivado desde el original el 2 de abril de 2015.
- ↑ Takhampunya R, Ubol S, Houng HS, Cameron CE, Padmanabhan R (2006). «Inhibition of dengue virus replication by mycophenolic acid and ribavirin». J. Gen. Virol. 87 (Pt 7): 1947-52. PMID 16760396. doi:10.1099/vir.0.81655-0. Archivado desde el original el 30 de abril de 2008. Consultado el 6 de abril de 2008.
- ↑ Guy, Bruno; Briand, Olivier; Lang, Jean; Saville, Melanie; Jackson, Nicholas (10 de diciembre de 2015). «Development of the Sanofi Pasteur tetravalent dengue vaccine: One more step forward». Vaccine. Dengue Vaccines 33 (50): 7100-7111. doi:10.1016/j.vaccine.2015.09.108. Consultado el 7 de julio de 2017.
- ↑ «Dengvaxia®, World’s First Dengue Vaccine, Approved in Mexico». www.sanofipasteur.com (en inglés). Archivado desde el original el 10 de diciembre de 2015. Consultado el 7 de julio de 2017.
- ↑ What is Dengvaxia and how is it used?. MedicineNer. Consultado el 30 de mayo de 2019.
- ↑ Dengvaxia. European Medicines Agency. Publicado el 18 de diciembre de 2018. Consultado el 30 de junio de 2019.
- ↑ «Dengue», artículo en el sitio web Monografías.com.
- ↑ Fernanda Pontes (20 de marzo de 2008), «Secretário estadual de Saúde Sérgio Côrtes admite que estado vive epidemia de dengue», O Globo Online (en portugués), archivado desde el original el 22 de julio de 2011..
- ↑ CNN (3 de abril de 2008), «Thousands hit by Brazil outbreak of dengue», CNN (en inglés)..
- ↑ Organización Mundial de la Salud. «Dengue/dengue hemorrágico en Brasil». Consultado el 21 de octubre de 2009.
- ↑ Unusual dengue virus 3 epidemic in Nicaragua, 2009. Gutierrez G, Standish K, Narvaez F, Perez MA, Saborio S, Elizondo Dina, Ortega O, Nuñez A, Kuan G, Balmaseda A, Harris E. Source Sustainable Sciences Institute, Managua, Nicaragua.
- ↑ «Página/12 :: El país :: Verano del ’96».
- ↑ Color, A. B. C. «Récord de muertes por dengue en Paraguay - Nacionales - ABC Color». www.abc.com.py. Consultado el 11 de mayo de 2019.
- ↑ http://scielo.iics.una.py/scielo.php?script=sci_arttext&pid=S2072-81742015000100003
- ↑ "Confirmados en Murcia dos casos de dengue contraído en España" El Mundo / Europa Press
- ↑ «Gobierno confirmó el tercer caso de dengue autóctono en Uruguay». www.elpais.com.uy. Consultado el 22 de febrero de 2016.
- ↑ «Brote de dengue en Pocitos y Malvín Norte». www.elobservador.com.uy. Consultado el 22 de febrero de 2016.
- ↑ «Vázquez confirmó detección del tercer caso de dengue autóctono en Pocitos». www.subrayado.com.uy. Consultado el 22 de febrero de 2016.
- ↑ Duggleby, Luke; Siegel, Laure (30 de diciembre de 2019). «Asia's hardest year for dengue fever – in pictures». The Guardian (en inglés). Consultado el 24 de mayo de 2020.
- ↑ Miranda, Boris (13 de febrero de 2020). «Por qué América Latina está registrando "la mayor epidemia de dengue de su historia"». BBC News. Consultado el 24 de mayo de 2020.
- ↑ «Grave: mientras crece el alerta por el coronavirus, en la región ya hay más de 600 mil casos de dengue y más de un centenar de muertos entre Brasil y Paraguay este año». MisionesOnline. 11 de marzo de 2020. Consultado el 18 de marzo de 2020.
- ↑ «Dengue: el gobierno de Milei no incluirá la vacuna en el calendario nacional». chacodiapordia.com. 4 de marzo de 2024. Consultado el 12 de abril de 2024.
- ↑ Vega, Matías (27 de marzo de 2024). «Argentina ya atraviesa la peor epidemia de dengue de su historia: más de 100 mil casos». Bio Bio Chile. Consultado el 29 de marzo de 2024.
- ↑ Soria, Horacio; Lo Bianco, Miguel; Corvalan, Javier (21 de marzo de 2024). «Dengue outbreak in Argentina on track to break records». Reuters (en inglés). Consultado el 29 de marzo de 2024.
- ↑ «Más de 440 muertos por dengue desde enero en Perú, su peor cifra en décadas». France 24. 28 de noviembre de 2023. Consultado el 10 de enero de 2024.
- ↑ a b Maguiña Vargas, Ciro (20 de abril de 2023). «El brote de dengue en Perú: Análisis y perspectivas». Acta Médica Peruana. Consultado el 10-01-2023.
- ↑ a b «Dengue, ¿próximo fin de la amenaza?». La Jornada. Pl. 10 de septiembre de 2011. Consultado el 11 de septiembre de 2011. (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última).
- ↑ «Chemical and biological weapons: possession and programs past and present», artículo en James Martin Center for Nonproliferation Studies, Middlebury College, 9 de abril de 2002. Consultado el 14 de noviembre de 2008.
Bibliografía[editar]
- Gubler DJ (2010). "Dengue viruses". In Mahy BWJ, Van Regenmortel MHV. Desk Encyclopedia of Human and Medical Virology. Boston: Academic Press. pp. 372–82. ISBN 0-12-375147-0.
- WHO (2009). Dengue Guidelines for Diagnosis, Treatment, Prevention and Control. Geneva: World Health Organization. ISBN 92-4-154787-1.
- Harrison. Principles of Internal Medicine. 18º Ed. McGraw Hill.
Enlaces externos[editar]
 Wikimedia Commons alberga una categoría multimedia sobre Dengue.
Wikimedia Commons alberga una categoría multimedia sobre Dengue. Wikinoticias tiene noticias relacionadas con Dengue.
Wikinoticias tiene noticias relacionadas con Dengue.- Texto acerca del dengue en el sitio web de la Universidad de Buenos Aires
- «Dengue», artículo en español en el sitio web de la Organización Mundial de la Salud.
- «Dengue y dengue hemorrágico», artículo en el sitio web de los Centros para el Control y la Prevención de Enfermedades.
- «Dengue», artículo en el sitio web Enciclopedia Médica Medline Plus.
- «Fiebre hemorrágica del dengue», artículo en el sitio web Enciclopedia Médica Medline Plus.
- Worldwide Mapping of Dengue Antiviral Research, 2010
- «Estudio de brote epidemiológico de dengue en San Antonio el Grande (Hidalgo)» (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última)., artículo en el sitio web de la Asociación Mexicana de Infectología y Microbiología Clínica. Consultado el 13 de octubre de 2012.
- Guía para el equipo de salud
