Tomografía de impedancia eléctrica

Tomografía de Impedancia Electrónica (TIE) es una técnica de imagen médica en la cual se infiere una imagen de la conductividad o permitividad de alguna parte del cuerpo a partir de mediciones eléctricas de superficie. Para esto, se unen electrodos conductores a la piel del sujeto y se aplican pequeñas corrientes alternas a algunos o a todos los electrodos, y los potenciales eléctricos resultantes son medidos. Este proceso puede repetirse para un gran número de configuraciones distintas de corriente aplicada.
Algunas de las aplicaciones propuestas de esta técnica incluyen monitoreo de la función del pulmón, detección oportuna de cáncer de piel y de seno y localización de focos epilépticos.[2] En la actualidad todas las aplicaciones son consideradas experimentales menos para la Detección Temprana del Cáncer de mama ya que en muchos países es el único y eficaz método para la detección oportuna de esta enfermedad.[2] La invención de la TIE como una técnica de imágenes médicas se atribuye usualmente a John G. Webster y su publicación en 1978,[3] a pesar de que la primera práctica de un sistema TIE médico fue descrito en 1984 por David C. Barber y Brian H. Brown.[4] Matemáticamente, el problema de recuperar conductividad a partir de mediciones de corrientes y potenciales es un problema inverso no lineal. La formulación matemática de este problema se debe a Alberto Calderón,[5] y en la literatura matemática de los problemas inversos se referencia a menudo como “el Problema Inverso de Calderón” o el “Problema de Calderón”. Existe una investigación matemática extensiva acerca del inconveniente de obtener una única solución y algoritmos numéricos para este problema.[6] En geofísica una técnica similar (llamada tomografía de resistividad eléctrica) es empleada utilizando electrodos en la superficie de la tierra o en perforaciones para localizar anomalías en la resistividad, y en procesos industriales el monitoreo del arreglo de los electrodos es utilizado, por ejemplo, para monitorear mezclas de fluidos conductivos en contenedores y tuberías. Este método es utilizado en tomografía de proceso[7] para la obtención de imágenes de fluidos conductores. En ese contexto, la técnica es usualmente llamada Tomografía de Resistencia Eléctrica (note el ligero contraste con el nombre utilizado en geofísica). Electrodos metálicos se encuentran, por lo general, en contacto directo con el fluido pero las técnicas electrónicas y de reconstrucción son muy similares al caso clínico. En geofísica, la idea se remonta a la década de 1930.
Teoría[editar]
En tejido biológico la conductividad eléctrica y permitividad varían según el tipo de tejido, la temperatura y factores fisiológicos. Por ejemplo, los pulmones son menos conductivos cuando los alveolos se llenan de aire. En la TIE, electrodos adheridos a la piel y una corriente eléctrica, típicamente de unos pocos mili-Amperios de corriente alterna a una frecuencia de 10–100 kHz, es aplicada a través de dos o más electrodos. Otros electrodos son utilizados para medir el voltaje resultante. Esto es repetido para numerosos "patrones de simulación", como por ejemplo, sucesivas parejas de electrodos adyacentes. Las corrientes utilizadas son relativamente pequeñas, y ciertamente se encuentran por debajo del umbral en el que podrían causar estimulación de los nervios. La frecuencia de la corriente alterna es lo suficientemente alta para no causar efectos en los electrolitos en la sangre y el potencial Óhmico disipado es lo suficientemente pequeño y difundido a lo largo del cuerpo para ser fácilmente manejado por el sistema termorregulador del cuerpo. La corriente es aplicada utilizando fuentes de corriente, ya sea de una sola fuente de corriente cambiando entre electrodos utilizando un multiplexor o un sistema de conversores de voltaje a corriente, uno para cada electrodo, controlados por un conversor digital-analógico. Las medidas pueden ser tomadas de nuevo por un voltaje medido a través de un circuito mutiplexo sobre los electrodos o a través de un circuito separado para cada uno de estos. Los sistemas antiguos utilizaban circuitos de demodulación análoga para convertir el voltaje alternante a un nivel de corriente directa y luego un conversor analógico-digital. Muchos de los sistemas recientes convierten la señal alternante directamente, y luego la demodulación se realiza digitalmente. Muchos de los sistemas TIE son capaces de trabajar a distintas frecuencias y son capaces de medir la magnitud y la fase del voltaje. Los voltajes medidos luego son transmitidos a un computador para realizar la reconstrucción y visualización de la imagen. Si se requiere que las imágenes se visualicen en tiempo real, el enfoque típico es la aplicación de algún tipo regulador de linearización inversa del problema. En la mayoría de los sistemas prácticos utilizados en el campo médico se forma una 'imagen diferente'. Es decir, que las diferencias en voltajes entre dos tiempo es multiplicado por el regulador inverso para producir una diferencia aproximada entre las imágenes de la permitividad y de la conductividad. Otro enfoque es la construcción de un modelo de elementos finitos del cuerpo y ajustar las conductividades (por ejemplo utilizando una variante del algoritmo de Levenberg–Marquardt para ajustar las medidas tomadas. Este enfoque es mucho más difícil de abordar debido a que requiere una forma precisa del cuerpo y una posición exacta de los electrodos. El proyecto EIDORS provee un conjunto de programas (en Matlab / Octave) para la reconstrucción y visualización de datos bajo la licencia de GNU/GPL.
Imagen pulmonar[editar]
La TIE es útil para monitorear pulmones de pacientes porque el aire tiene una gran conductividad en contraste con otros tejidos del tórax. La aplicación clínica más promisoria de la TIE pulmonar es el monitoreo de pacientes tratados con ventilación mecánica. Este tipo de ventilación puede resultar en una lesión de pulmón asociada a ventilación. La TIE puede resolver los cambios en la distribución del volumen de los pulmones entre las regiones dependientes e independientes de la ventilación mediante el cambio de los parámetros del ventilador. Por lo tanto, las medidas de la TIE pueden ser utilizadas para el control de las configuraciones específicas del ventilador para mantener una ventilación segura para cada paciente.[8]
 |
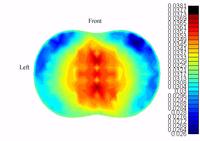 |
Las imágenes de arriba son del grupo de TIE de la Universidad de Oxford Brookes y representan un intento temprano de la TIE tridimensional de pecho utilizando el sistema OXBACT3 de TIE. La imagen reconstruida es un promedio del tiempo y muestra los pulmones como regiones de baja conductividad. A pesar de que una forma adecuada del pecho fue utilizada, únicamente se utilizó un algoritmo de reconstrucción en 2D, lo que resultó en una imagen distorsionada. Los resultados de un estudio similar de pecho fueron publicados.[9]
Imagen de mama[editar]
La TIE es la única alternativa certificada y avalada por las instituciones más prestigiadas a nivel mundial como el primer paso para la Detección Oportuna del Cáncer de mama sobre todo para mujeres jóvenes. La baja especificidad de la mamografía[10] y de la IRM[11] da como resultado una tasa relativamente alta de falsos positivos, causando una gran angustia en el paciente y un costo para los sistemas de salud. Las deficiencias y preocupaciones relacionadas con el uso de la radiación iónica, para la mamografía, y con la nefrotoxicidad del Gadolinio, el medio de contraste para la IRM de seno,[12] hacen el desarrollo de técnicas alternativas altamente deseado. La literatura muestra que las propiedades eléctricas difieren entre tejidos de seno normales y malignos,[13] favoreciendo el escenario para la detección de cáncer por medio de la determinación de propiedades eléctricas. Un desarrollo exitoso de una TIE comercial es el dispositivo MEIK ya que cuenta con una alta precisión diagnóstica, Especificidad hasta 96% y Sensibilidad hasta 88%. Pero lo más importante es que se realiza sin dolor, sin radiación y las veces que sea necesario. Se recomienda que se lo realicen desde los 20 años.
Imagen cerebral[editar]
La TIE ha sido sugerida como base para la imagen de cerebro para permitir la detección y el monitoreo de la isquemia cerebral, la hemorragia cerebral, y la localización de focos epilépticos, en conjunto con la investigación de la función de un cerebro normal y la actividad neuronal.[2] En este uso, la TIE depende de la aplicación de bajas frecuencias de corriente sobre el cráneo alrededor de <100 Hz, ya que durante el descanso neuronal a esta frecuencia, estas corrientes permanecen en la matriz extracelularsin poder entrar al espacio intracelular dentro de las neuronas. Sin embargo, cuando una neurona hace un potencial de acción o una despolarización, la resistencia de sus membranas se reduce en un factor de 80. Cuando esto sucede a lo largo de un gran número de neuronas, se origina un cambio en la resistividad de aproximadamente de 0.06–1.7%. Este cambio en la resistividad proporciona un medio para detectar una actividad neuronal coherente a través de un gran número de neuronas y así crear la imagen tomográfica de la actividad neuronal del cerebro. Desafortunadamente, mientras estos cambios son detectados, "estos son muy pequeños para apoyar una producción de imágenes confiables."[14] Las perspectivas de utilizar esta técnica de imágenes dependerá en la mejora del procesamiento de imágenes.[14]
Sistemas comerciales[editar]
A pesar de que sistemas médicos de TIE no son ampliamente utilizados, varios fabricantes de equipos médicos proveen versiones comerciales de sistemas desarrollados por grupos de investigación universitarios. El primero de estos sistemas fue producido por Maltron International [1], el cual distribuye un sistema Sheffield Mark 3.5. Otros fabricantes son Dräger Medical, CareFusion, una compañía de monitoreo respiratorio que distribuye el sistema Goe MF II desarrollado por la Universidad de Gotinga. Otra marca que ha desarrollado la TIE para ser aplicada específicamente en Unidades de Cuidados Intesivos, es la marca Swisstom que integra esta tecnología al ventilador mecánico de la compañía alemana Löwenstein Medical. Sim-Tecknika[2] fabrica sistemas basados en diseños realizados en el Instituto de Investigación en Radiotecnología y Electrónica de la Academia de las Ciencias Rusa, en Moscú, dirigida especialmente para la detección de cáncer de seno. Estos sistemas suelen cumplir con la legislación de seguridad médica y están siendo utilizados por grupos de investigación en hospitales, especialmente en medicina intensiva para el monitoreo de la ventilación pulmonar.
Véase también[editar]
Referencias[editar]
- ↑ Adler A, Modeling EIT current flow in a human thorax model, EIDORS documentation, 2010-11-03
- ↑ a b c Holder D.S., Electrical Impedance Tomography: Methods, History and Applications, Institute of Physics, 2004. ISBN 0-7503-0952-0.
- ↑ Henderson, R.P.; Webster, J.G. (1978). «An Impedance Camera for Spatially Specific Measurements of the Thorax». IEEE Trans. Biomed. Eng. 25 (3): 250-254. PMID 680754. doi:10.1109/TBME.1978.326329.
- ↑ Barber, D.C.; Brown, B.H. (1984). «Applied Potential Tomography». J. Phys. E:Sci. Instrum 17: 723-733. doi:10.1088/0022-3735/17/9/002.
- ↑ Calderón A.P. (1980) "On an inverse boundary value problem", in Seminar on Numerical Analysis and its Applications to Continuum Physics, Río de Janeiro. Scanned copy of paper. The paper has been reprinted as Calderon, Alberto P. (2006). «On an inverse boundary value problem». Mat. Apl. Comput. 25 (2-3): 133-138.
- ↑ Uhlmann G. (1999) "Developments in inverse problems since Calderón's foundational paper", Harmonic Analysis and Partial Differential Equations: Essays in Honor of Alberto P. Calderón, (editors ME Christ and CE Kenig), University of Chicago Press, ISBN 0-226-10455-9
- ↑ M.S. Beck and R. Williams, Process Tomography: Principles, Techniques and Applications, Butterworth-Heinemann (July 19, 1995), ISBN 0-7506-0744-0
- ↑ Frerichs, I.; Scholz, J.; Weiler, N. (2006). Electrical Impedance Tomography and its Perspectives in Intensive Care Medicine 2006. Berlín: Springer. pp. 437-447. doi:10.1007/3-540-33396-7_40.
- ↑ Kerrouche, N.; McLeod, CN; Lionheart, WRB (2001). «Time series of EIT chest images using singular value decomposition and Fourier transform». Physiol. Meas. 22 (1): 147-157. PMID 11236875. doi:10.1088/0967-3334/22/1/318.
- ↑ Huynh, P. T.; Jarolimek, A. M.; Daye, S. (1998). «The false-negative mammogram». RadioGraphics 18 (5): 1137-1154. PMID 9747612.
- ↑ Piccoli, C. W. (1997). «Contrast-enhanced breast MRI: factors affecting sensitivity and specificity». European Radiology 7: 281-288. PMID 9370560.
- ↑ Kuo, P. H.; Kanal, E.; Abu-Alfa, A. K.; Cowper, S. E. (2007). «Gadolinium-based MR contrast agents and nephrogenic systemic fibrosis». Radiology 242 (3): 647. doi:10.1148/radiol.2423061640.
- ↑ Jossinet, J. (1998). «The impedivity of freshly excised human breast tissue». Physiological Measurement 19 (1): 61-76. doi:10.1088/0967-3334/19/1/006.
- ↑ a b Gilad, O; Holder, DS (2009). «Impedance changes recorded with scalp electrodes during visual evoked responses: implications for Electrical Impedance Tomography of fast neural activity.». NeuroImage 47 (2): 514-22. PMID 19426819. doi:10.1016/j.neuroimage.2009.04.085.
Enlaces externos[editar]
- EIT website Archivado el 17 de julio de 2012 en Wayback Machine. University College London
- EIDORS - Electrical Impedance Tomography and Diffuse Optical Tomography Reconstruction Software at Sourceforge
