Efectos del disolvente
En química, los efectos del disolvente son un grupo de efectos que un disolvente dado tiene sobre la reactividad química. Los disolventes pueden tener un efecto en la solubilidad, estabilidad y velocidad de reacción, así que la elección del disolvente apropiado permite el control cinético y termodinámico en una reacción química.
Efectos sobre la solubilidad[editar]
Un soluto se disuelve en un disolvente cuando forma interacciones favorables con el disolvente. La disolución depende del cambio en la energía libre, tanto del soluto como del disolvente. La energía libre de solvatación es una combinación de varios factores.
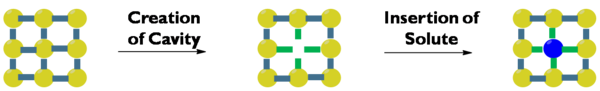
Primero debe crearse una cavidad en el disolvente. La creación de dicha cavidad será entrópicamente y entálpicamente desfavorable, dado que las moléculas del disolvente se localizan en regiones más pequeñas, y hay menos interacciones disolvente-disolvente. Segundo, el soluto debe separarse de las partículas grandes de soluto. Esto es entálpicamente desfavorable, puesto que se rompen interacciones soluto-soluto, pero entrópicamente favorable. Tercero, el soluto debe ocupar la cavidad creada en el disolvente. Esto resulta en interacciones soluto-disolvente favorables, y es entrópicamente favorable puesto que la mezcla está más desordenada que cuando el disolvente y el soluto no estaban mezclados. La disolución se da frecuentemente cuando las interacciones soluto-disolvente son similares a las interacciones disolvente-disolvente, lo que se refleja en la expresión lo semejante disuelve a lo semejante.[1] De ahí que los solutos polares se disuelvan en disolventes polares, mientras que los solutos no polares se disuelven en disolventes no polares. No hay una sola medida de la polaridad del disolvente, así que la clasificación de los disolventes basada en la polaridad puede llevarse a cabo usando diferentes escalas. (ver también: Disolvente - clasificación de los disolventes)
Efectos en la estabilidad[editar]
Diferentes disolventes pueden afectar la constante de equilibrio de una reacción por estabilización diferencial del reactante o el producto. El equilibrio es empujado en la dirección de la sustancia que es estabilizada preferentemente. La estabilización del reactante o producto puede darse a través de cualquiera de las interacciones no covalentes con el disolvente, tales como el enlace de hidrógeno, interacciones dipolo-dipolo, etc.
Equilibrio ácido-base[editar]
El equilibrio de ionización de un ácido o una base está afectado por un cambio en el disolvente. El efecto del disolvente no es sólo debido a su acidez o basicidad, sino también a su constante dieléctrica y su habilidad para solvatar preferentemente y entonces estabilizar ciertas especies en el equilibrio ácido-base. Entonces, un cambio en la habilidad de solvatación o constante dieléctrica puede influir en la acidez o basicidad.
| Disolvente | Constante dieléctrica[2] |
|---|---|
| Acetonitrilo | 37 |
| Dimetil sulfóxido | 47 |
| Agua | 78 |
En la tabla anterior puede verse que el agua es el disolvente más polar, seguido por el DMSO y luego el acetonitrilo. Considérese el siguiente equilibrio de disociación ácido:
- HA
 A− + H+,
A− + H+,
El agua, al ser el disolvente más polar listado anteriormente, estabiliza las especies iónicas en mayor grado de lo que lo hacen el DMSO o el acetonitrilo. La ionización, y en consecuencia la acidez, será más grande en el agua, y menor en el DMSO y el acetonitrilo, como se puede ver en la tabla siguiente, que muestra los valores de pKa a 25.oC para el acetonitrilo (ACN)[3][4][5] y dimetilsulfóxido (DMSO)[6] and water.
| HA |
ACN | DMSO | agua |
|---|---|---|---|
| Ácido p-toluenosulfónico | 8.5 | 0.9 | fuerte |
| 2,4-Dinitrofenol | 16.66 | 5.1 | 3.9 |
| Ácido benzoico | 21.51 | 11.1 | 4.2 |
| Ácido acético | 23.51 | 12.6 | 4.756 |
| Fenol | 29.14 | 18.0 | 9.99 |
Equilibrio ceto-enol[editar]
Varios compuestos 1,3-dicarbonílicos pueden existir en las siguientes formas tautoméricas como se muestra a continuación.
Los compuestos 1,3-dicarbonílicos sufren una tautomerización frecuente entre la forma cíclica enólica (conocida como la forma cis) y la forma diceto. La constante de equilibrio para la tautomerización está dada por:
El efecto del disolvente sobre la constante de equilibrio de tautomerización de la acetilacetona es como sigue:
| Disolvente | KT |
|---|---|
| Fase gaseosa | 11.7 |
| Ciclohexano | 42 |
| Tetrahidrofurano | 7.2 |
| Benceno | 14.7 |
| Etanol | 5.8 |
| Diclorometano | 4.2 |
| Agua | 0.23 |
La forma cis enólica predomina en disolventes de baja polaridad, mientras que la forma diceto predomina en disolventes de alta polaridad. El enlace de hidrógeno intramolecular formado en la forma cis está más pronunciado cuando no hay una competencia para la formación de un enlace de hidrógeno intermolecular con el disolvente. Como resultado, los disolventes de baja polaridad que no forman enlaces de hidrógeno fácilmente permiten la estabilización de la forma cis enólica por enlace de hidrógeno intramolecular.
Efectos en la velocidad de las reacciones[editar]
Frecuentemente, se esquematizan la reacitividad y los mecanismos de reacción como el comportamiento de moléculas aisladas en el cual el disolvente es tratado como un soporte pasivo. Sin embargo, los disolventes pueden influir realmente en la velocidad de las reacciones y el orden de una reacción química.[7][8][9][10]
Efectos del disolvente sobre el equilibrio[editar]
Los disolventes pueden afectar las velocidades a través de los efectos del disolvente en el equilibrio, lo que puede ser explicado a partir de la teoría del estado de transición. Esencialmente, la velocidad de las reacciones están influenciada por la solvatación diferencial del material inicial y el estado de transición por el disolvente. Cuando las moléculas del reactante proceden hacia el estado de transición, las moléculas de disolvente se orientan para estabilizar el estado de transición. Si el estado de transición es estabilizado en mayor medida que el material inicial, la reacción procede más rápidamente. Si el material inicial es estabilizado en mayor medida que el estado de transición, la reacción procede más lentamente. Sin embargo, dicha solvatación diferencial requiere una rápida relajación reorientacional del disolvente (de la orientación del estado de transición de vuelta hacia la orientación del estado fundamente). En consecuencia, los efectos del disolvente en el equilibrio se observan en reacciones que tienden a tener barreras altas, y solvntes débilmente dipolares, que se relajan rápidamente.[7]
Efectos friccionales del disolvente[editar]
La hipótesis del equilibrio no responde adecuadamente las reacciones químicas muy rápidas, en las que la teoría del estado de transición falla. En tales casos que involucran un disolvente fuertemente dipolar, de relajación lenta, la solvatación del estado de transición no juega un rol significativo en afectar la velocidad de reacción. En su lugar, las contribuciones dinámicas del disolvente (tales como la fricción, densidad, presión interna o viscosidad) juegan un rol más significativo en cómo afectan la velocidad de la reacción.[7][10]
Reglas de Hughes-Ingold[editar]
Los efectos del disolvente en las reacciones de sustitución nucleofílica y eliminación fueron estudiados originalmente por Hughes e Ingold. Mediante el uso de un modelo de solvatación simple que sólo consideraba interacciones electrostáticas puras entre los iones o moléculas dipolares, y los disolventes en el estado inicial y de transición, organizaron todas las reacciones nucleofílicas y de eliminación en tipos de carga diferentes (cargados negativamente, positivamente, o neutros).[7] A continuación, Hughes e Ingold elaborarion ciertas suposiciones que podían hacerse acerca del grado de solvatación que podía esperarse en estas situaciones:
- un incremento en la magnitud de la carga aumentará la solvatación
- un incremento en la deslocalización disminuirá la solvatación
- la pérdida de carga disminuirá la solvatación, más que la dispersión de la carga[7]
El efecto aplicativo de estas suposiciones generales se muestra en los siguientes ejemplos:
- Un incremento en la polaridad del disolvente acelera la velocidad de las reacciones donde se desarrolla una carga en el completo activado, a partir de reactantes neutros o ligeramente cargados
- Un incremento en la polaridad del disolvente disminuye la velocidad de las reacciones donde hay una pérdida de carga en el complejo activado, en comparación a los materiales iniciales
- Un cambio en la polaridad del disolvente tendrá poco o ningún efecto sobre la velocidad de las reacciones cuando hay poca o ninguna diferencia en la carga entre los reactantes y el complejo activado.[7]
Ejemplos de reacción[editar]
Reacciones de sustitución[editar]
El disolvente usado en las reacciones de sustitución determina inherentemente la nucleofilicidad del nucleófilo; este hecho se ha vuelto más evidente puesto que más reacciones son llevadas a cabo en fase gaseosa.[11] Así, las condiciones del disolvente impactan significativamente en el rendimiento de una reacción, con ciertas condiciones de disolvente favoreciendo un mecanismo de reacción sobre otro. Para las reacciones SN1, la habilidad de los disolventes para estabilizar el carbocatión intermediario es de importancia directa para su viabilidad como un disolvente apropiado. La habilidad de los disolventes polares para incrementar la velocidad de las reaccionesSN1 es un resultado de los disolventes polares solvatando a las especies reactantes intermedias, esto es, al carbocatión, con lo que se disminuye la energía intermedia relativa al material inicial. La siguiente tabla muestra las velocidades de solvólisis de cloruro de tert-butilo con ácido acético, metanol y agua.
| Disolvente | Constante dieléctrica, ε | Velocidad relativa |
|---|---|---|
| CH3CO2H | 6 | 1 |
| CH3OH | 33 | 4 |
| H2O | 78 | 150,000 |
El caso de las reacciones SN2 es algo diferente, puesto que la ausencia de solvatación del nucleófilo incrementa la velocidad de una reacción SN2. En cualquier caso (SN1 o SN2), la habilidad de estabilizar el estado de transición (SN1) o desestabilizar el material reactante inicial ((SN2) actúa para disminuir la energía de activación, incrementando la velocidad de la reacción. Esta relación es acorde con la ecuación ΔG = -RT ln K (energía libre de Gibbs). La ecuación de velocidad para las reacciones SN2 es bimolecular, siendo de primer orden en el nucleófilo, y de primer orden en el reactivo. El factor determinante cuando tanto los mecanismos SN1 y SN2 son viables es la fuerza del nucleófilo. La nucleofilicidad y basicidad están relacionadas, y mientras más nucleofílica se vuelve una molécula, más grande se hace la basicidad del nucleófilo. Este incremento en la basicidad ocasiona problemas a los mecanismos de reacción SN2, cuando el disolvente de elección es prótico. Los disolventes próticos reaccionan con nucleófilos fuertes con buen carácter básico, mediante el esquema ácido/base, con lo que se disminuye o elimina la naturaleza nucleofílica del nucleófilo. La siguiente table muestra el efecto de la polaridad del disolvente en las velocidades de reacción relativas de la reacción SN2 del bromuro de n-butilo con anión azida, N3 −. Obsérvese el gran aumento en la velocidad de la reacción cuando se cambia de un disolvente prótico a uno aprótico. Esta diferencia surge de las reacciones ácido/base entre los disolventes próticos (que no se da con los disolventes apróticos) y los nucleófilos fuertes. Es importante observar también que tanto los efectos de disolvente como los efectos estéricos impactan en las velocidades de reacción relativas.
- [12] sin embargo, para los casos mostrados a continuación en la demostración de las velocidades de reacción SN2, los efectos estéricos pueden ser despreciados.
| Disolvente | Constante dieléctrica, ε | Velocidad relativa | Tipo |
|---|---|---|---|
| Metanol | 33 | 1 | Prótico |
| Agua | 78 | 7 | Prótico |
| Dimetil sulfóxido | 49 | 1,300 | Aprótico |
| Dimetilformamida | 37 | 2800 | Aprótico |
| Yoduro de metilo | 38 | 5000 | Aprótico |
Referencias[editar]
- ↑ Eric V. Anslyn; Dennis A. Dougherty (2006). Modern Physical Organic Chemistry. University Science Books. ISBN 978-1-891389-31-3.
- ↑ Plantilla:Loudon p. 317–318
- ↑ Kütt, A.; Movchun, V.; Rodima, T,; Dansauer, T.; Rusanov, E.B.; Leito, I.; Kaljurand, I.; Koppel, J.; Pihl, V.; Koppel, I.; Ovsjannikov, G.; Toom, L.; Mishima, M.; Medebielle, M.; Lork, E.; Röschenthaler, G-V.; Koppel, I.A.; Kolomeitsev, A.A. (2008). «Pentakis(trifluoromethyl)phenyl, a Sterically Crowded and Electron-withdrawing Group: Synthesis and Acidity of Pentakis(trifluoromethyl)benzene, -toluene, -phenol, and -aniline». J. Org. Chem. 73 (7): 2607-2620. doi:10.1021/jo702513w.
- ↑ Kütt, A.; Leito, I.; Kaljurand, I.; Sooväli, L.; Vlasov, V.M.; Yagupolskii, L.M.; Koppel, I.A. (2006). «A Comprehensive Self-Consistent Spectrophotometric Acidity Scale of Neutral Brønsted Acids in Acetonitrile». J. Org. Chem. 71 (7): 2829-2838. doi:10.1021/jo060031y.
- ↑ Kaljurand, I.; Kütt, A.; Sooväli, L.; Rodima, T.; Mäemets, V. Leito, I; Koppel, I.A. (2005). «Extension of the Self-Consistent Spectrophotometric Basicity Scale in Acetonitrile to a Full Span of 28 pKa Units: Unification of Different Basicity Scales». J. Org. Chem. 70 (3): 1019-1028. doi:10.1021/jo048252w.
- ↑ «Bordwell pKa Table (Acidity in DMSO)». Consultado el 2 de noviembre de 2008.
- ↑ a b c d e f Reichardt, Christian (1990). Solvent Effects in Organic Chemistry. Marburg, Germany: Wiley-VCH. pp. 147–181. ISBN 0895736845.
- ↑ Jones, Richard (1984). Physical and Mechanistic Organic Chemistry. Cambridge: Cambridge University Press. pp. 94–114. ISBN 0521226422.
- ↑ James T. Hynes (1985). «Chemical Reaction Dynamics in Solution». Ann. Rev. Phys. Chem 36: 573-597.
- ↑ a b Sundberg, Richard J.; Carey, Francis A. (2007). Advanced Organic Chemistry: Structure and Mechanisms. Nueva York: Springer. pp. 359–376. ISBN 978-0387448978.
- ↑ Eğe, Seyhan (2008). Organic Chemistry Structure and Reactivity. Houghton Mifflin Harcourt. ISBN 0618318097.
- ↑ Yongho, Kim.; Cramer, Christopher J.; Truhlar, Donald G. (2009). «Steric Effects and Solvent Effects on SN2 Reactions». J. Phys. Chem. A 113: 9109-9114. doi:10.1021/jp905429p.

![{\displaystyle {\mathbf {K} }_{\mathrm {T} }={\frac {[cis-enol]}{[diceto]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/70f34b3d12ce717d5e189a7bdcf7fd1f9845e2f5)