Dolichonyx oryzivorus
| Dolichonyx oryzivorus | ||
|---|---|---|
 Macho en plumaje nupcial. | ||
| Estado de conservación | ||
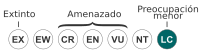 Preocupación menor (UICN 3.1)[1] | ||
| Taxonomía | ||
| Reino: | Animalia | |
| Filo: | Chordata | |
| Clase: | Aves | |
| Orden: | Passeriformes | |
| Familia: | Icteridae | |
| Género: |
Dolichonyx Swainson, 1827[2][3] | |
| Especie: |
D. oryzivorus (Linnaeus, 1758)[1][4] | |
| Distribución | ||
| Anaranjado: fuera de la época de reproducción. | ||
| Sinonimia | ||
El charlatán (Dolichonyx oryzivorus), también conocido como tordo charlatán,[5] chambergo,[6] tordo arrocero,[7] triste-pía,[7] canadiense,[4] o chupador,[4][8][nota 1] es una especie de ave paseriforme de la familia Icteridae propia de América. Es el único miembro del género Dolichonyx. Es un pájaro de hábitos migratorios que vuela anualmente desde las regiones templadas de América del Norte hasta Sudamérica centromeridional. Es conocido por tener la ruta migratoria más larga de todas las aves terrestres del continente americano.[9][10] Se trata de una especie poligínica y gregaria, que se alimenta de diversos tipos de granos, incluyendo el arroz, lo que llevó a que fuera considerada una plaga en algunas áreas; también consume insectos. Durante la temporada reproductiva, exhibe un marcado dimorfismo sexual que luego se disipa cuando el macho muda su plumaje por uno similar al de la hembra, poco antes de emprender su viaje al sur.[11] Es uno de los pocos paseriformes que experimentan dos mudas de plumas anuales, cambiando su plumaje completo tanto en América del Norte como del Sur.[4][7] Los charlatanes son aves de gran longevidad: viven comúnmente cinco o seis años.[12] A pesar de que su número va en descenso, es considerado una especie bajo preocupación menor.[1][7]
Taxonomía[editar]

El charlatán pertenece a la familia Icteridae, que comprende a aves paseriformes oriundas de América del Norte y del Sur. Constituye un género monotípico —Dolichonyx—, lo cual significa que es la única especie clasificada dentro del mismo. El pariente más cercano del charlatán probablemente sea el tordo cabeciamarillo (Xanthocephalus xanthocephalus); estas dos especies junto con el género Sturnella —filogenéticamente un poco más distanciado— integran la subfamilia Sturnellinae, un taxón basal dentro de la familia de los ictéridos.[13]
El charlatán fue descrito como especie por Carlos Linneo en 1758 en la décima edición de su obra Systema naturae bajo el nombre científico de Fringilla oryzivora.[3][14] Posteriormente, en 1827, William Swainson reemplazó esta denominación por la de Dolichonyx oryzivorus.[3] Robert Ridgway describió la subespecie Dolichonyx oryzivorus albinucha,[15] correspondiente a las poblaciones occidentales,[16] en contraposición a la subespecie nominal linneana (D. o. oryzivorus); pero luego, en 1894, la validez de estas subespecies fue anulada por la Unión Ornitológica Americana y actualmente se considera al charlatán una especie monotípica.[15][17] Su nombre específico, oryzivorus, significa «comedor de arroz» en latín. Sin embargo, este nombre, instituido por Linneo en 1758, es previo al advenimiento de las arroceras en América como recurso alimenticio para la población humana y, según se cree, hace referencia a otras plantas de la familia del arroz más que al arroz propiamente dicho (Oryza sativa), pues su adopción data de antes de que el ave comenzara a ser considerada una plaga para ese cultivo.[4]
Descripción[editar]

El plumaje nupcial de los machos es predominantemente negro, con la nuca de color crema y la parte baja del dorso, el obispillo y las plumas escapulares (aquellas que cubren la base del ala) blancos,[11][18] siendo la única ave en Estados Unidos con el vientre negro y el lomo blanco y no al revés.[19] Cuando los machos acaban de mudar sus plumas en Sudamérica por su plumaje nupcial antes de emigrar al norte, sus nuevas plumas exhiben unas puntas amarillentas que luego desaparecen, dejando al descubierto la coloración negra y blanca.[7][20] Fuera de la época de reproducción, se asemejan a las hembras.[21] Estas presentan una coloración beige en la cabeza y la parte baja, con dos gruesas franjas marrones oscuras sobre la cabeza que forman una especie de corona, vetas postoculares del mismo color y un veteado negruzco sobre los flancos; la parte superior es entre marrón y beige con un veteado negruzco; las alas y la cola son marrones negruzcas, bordeadas de beige y marrón.[22] La discreta coloración de las hembras las ayuda a camuflarse mientras anidan.[11] Los polluelos de ambos sexos se asemejan entre sí y se diferencian de un ave mayor por tener todo su plumaje, particularmente por debajo, de un color más amarillento; presentan un collar de débiles manchas oscuras sobre el pecho y el veteado lateral es casi indistinguible. Este plumaje pronto es reemplazado por otro en el que las listas negras de los flancos se vuelven claras y bien definidas y una mancha negra ocasionalmente aparece sobre las plumas de la garganta. En invierno este plumaje pierde gran parte de su brillo a causa del desgaste y el juvenil se parece mucho entonces a la hembra reproductiva.[23]
Los charlatanes son más pequeños que la mayoría de los ictéridos.[24] En promedio, pesan 28 gramos y miden de 16 a 18 cm.[4][18] Los machos pesan alrededor de un 9% más que las hembras.[25] La cola es corta y el pico, corto y cónico.[7] Las hembras y los juveniles presentan una coloración pálida en las patas y el pico —siendo más oscura la línea que se extiende entre el punto donde el maxilar superior emerge de la frente y la punta de dicho maxilar—;[7][22] los machos adultos exhiben picos negros y patas oscuras durante la temporada reproductiva, pero estos se tornan rosados fuera de la época de reproducción.[22][26] Las alas y las plumas de la cola son puntiagudas.[11][22][26]
Distribución[editar]
Se reproduce en América del Norte de mayo a julio entre los paralelos 40 y 50 y migra a Sudamérica para pasar allí los meses de noviembre a marzo entre los paralelos 8 y 32.[27] Su área de reproducción incluye pastizales abiertos y campos de heno en gran parte del sur de Canadá y del norte de Estados Unidos y abarca alrededor de 3,8 millones de km².[4] El charlatán está mayormente restringido a una franja de unos 800 km desde Nuevo Brunswick y Nueva Jersey central hasta Saskatchewan y Nebraska; hacia el oeste y noroeste existen poblaciones reproductivas más pequeñas esparcidas en ubicaciones muy distanciadas unas de otras, con extensas áreas de territorios no habitados en medio.[9] Estas aves vuelan a los humedales de las vastas llanuras de Bolivia,[18][28] el sudoeste de Brasil, Paraguay y el norte de Argentina para pasar allí los meses de primavera y verano australes entre noviembre y marzo.[21][29]
Migración[editar]

Aunque los charlatanes viajan grandes distancias, rara vez han sido vistos en Europa; como sucede con muchas otras aves oriundas de América del Norte, la gran mayoría de estos avistamientos de divagantes se produjo en las islas británicas.[18][28] Charles Darwin halló en octubre de 1835 un ejemplar en la Isla Santiago, en las Galápagos, distante casi mil kilómetros de Sudamérica continental.[16]
Sus rutas migratorias son complejas, irregulares y no del todo bien conocidas.[9] Viaja más de noche, pero no es un migrador estrictamente nocturno: vuela parcialmente durante el día tanto en otoño como en primavera.[9] Usa el campo magnético terrestre y los patrones estelares para guiarse.[10][21] La nubosidad podría interferir con la capacidad de orientación de estas aves.[9] El charlatán presenta la ruta migratoria más larga de todas las aves terrestres del continente americano,[9][10] volando alrededor de 20 000 km cada año,[4][7][21] y constituye el único ictérido migrador neártico que llega hasta Argentina.[29] Se comprobó que una hembra había alcanzado al menos los nueve años de edad, lo cual implicaba que las migraciones anuales a lo largo de su vida equivalían a cuatro vueltas y media a la tierra.[4][7]
Tras la finalización del ciclo reproductivo a mediados de julio, los charlatanes se reúnen localmente en las cercanías de áreas pantanosas, en donde mudan sus plumas, y a principios de agosto emprenden la migración de otoño.[9] El movimiento inicial es aparentemente hacia el sudeste, al menos para el grueso de las poblaciones orientales, y de mediados de agosto a mediados de septiembre grandes concentraciones son observadas a lo largo de la costa este desde Nueva Jersey hasta Florida.[9][30] Las observaciones de Clinton H. Merriam indican que arriban a los arrozales de Carolina del Sur y Georgia entre el 15 y el 21 de agosto y allí permanecen varias semanas sin avanzar.[16] En su migración a Sudamérica, las poblaciones occidentales aisladas parecerían desandar primero las supuestas rutas de colonización que, según la mayoría de los ornitólogos, las habrían llevado al oeste de América del Norte, volando en principio hacia el este, para luego dirigirse al sur.[9][21][30] La ausencia de avistamientos regulares en Arizona, Nuevo México y Texas sugiere que la ruta más directa para esas poblaciones a través de México es ignorada.[9]

La ruta migratoria continúa desde el sudeste de Estados Unidos a través del Caribe hacia Sudamérica, con paradas en Cuba y Jamaica.[9][21] En Cuba, Juan C. Gundlach registró su llegada en septiembre en inmensas bandadas, que permanecían solo durante un corto período antes de retomar su viaje al sur. Desde esa isla, Frank M. Chapman (1890) identifica tres rumbos distintos entre los que los charlatanes en migración pueden optar: siguiendo la costa occidental cubana, cruzando a Cozumel y a la península de Yucatán y a lo largo de la costa centroamericana en dirección a Panamá; al este a través de Haití, República Dominicana y Puerto Rico y desde allí hacia el sur a través de las Antillas Menores; o cruzando el mar directamente hacia Jamaica para luego, en un solo vuelo sostenido, alcanzar la costa norte de Sudamérica continental. Comparativamente pocos individuos parecen viajar tan hacia el este como para atravesar las Antillas Menores.[16] También Hamilton (1962) destacó que al este de Cuba y Jamaica los charlatanes se volvían cada vez más escasos y Alexander Wetmore manifestó que eran poco comunes en Puerto Rico durante la migración.[9] Sin embargo, algunos ejemplares han sido avistados en las Bermudas en lo que pareciera ser un viaje sin escalas desde las regiones costeras comprendidas entre Virginia y Nueva Escocia a Sudamérica.[21] Respecto de la procedencia de los individuos encontrados en Yucatán y Puerto Rico, Hamilton (1962) sugiere una interpretación alternativa, a saber, que esas aves estarían volando directamente a través del Caribe sin haber partido del sudeste de Estados Unidos.[9] Philip H. Gosse documentó el arribo en octubre de vastas cantidades de charlatanes a Jamaica que permanecían hasta comienzos de noviembre; otras observaciones indican que las aves se quedan en la isla por pocos días.[16] Aparentemente, la especie es nómada en su área de distribución sudamericana y la migración al sur podría no estar completa sino hasta enero.[9]
Los charlatanes emprenden su migración al norte a comienzos de abril, aunque algunos individuos pueden quedarse en sus cuarteles invernales hasta mayo.[16] En la temporada estival austral de 2009-2010, se constató que grandes cantidades de ellos se encontraban aún en el este de la provincia de Santa Fe hasta al menos el 31 de marzo y, aunque para la segunda quincena de abril casi la totalidad de las aves había abandonado las arroceras de la región, se registraron algunos ejemplares dispersos en una arrocera el 21 de abril, la fecha más tardía de avistamiento de charlatanes en la zona.[4] Desde Colombia y Venezuela, la mayoría continúa a través del mar Caribe hacia Florida,[16][21] aunque otros cruzan el golfo de México desde la península de Yucatán hacia Luisiana y Texas.[21] Gosse registró su regreso a Jamaica en abril, pero permanecían allí corto tiempo. Gundlach constató su arribo a Cuba en mayo y detalló que se quedaban en la isla por pocos días. Otros ingresan a Estados Unidos desde las Bahamas, donde están únicamente de paso y apenas paran a descansar.
La abundancia de alimento en el sur de Estados Unidos retrasa la llegada de algunos charlatanes a su área reproductiva. En Gainesville (Florida), Chapman encontró individuos de ambos sexos en grandes cantidades, alimentándose en campos de avena tan tarde como el 25 de mayo, y Merriam documentó la frecuente visita de las aves a los arrozales de Carolina de Sur y Georgia hasta el 29 de mayo, fecha para la cual la migración está próxima a su completitud y algunos charlatanes ya se han establecido en sus territorios de reproducción.[16] En el estado de Nueva York, por ejemplo, los machos regresan a las áreas reproductivas a comienzos de mayo y las hembras arriban alrededor de una semana después.[31][32]
Hábitat[editar]

Los charlatanes viven en hábitats agrícolas de baja intensidad productiva, como henares y pasturas, durante la temporada reproductiva. Asimismo, puede encontrárseles en campos exuberantes en barbecho y prados de pastos, herbáceas y flores silvestres. Los nidos son construidos a menudo en las áreas de mayor densidad y altura vegetativa. Aunque pequeños números pueden anidar en pastizales de entre 2 y 4 hectáreas, los campos de mayor extensión sustentan densidades más altas de parejas reproductivas. Utilizan hábitats similares a lo largo de su ciclo anual. Durante la migración, los charlatanes ocupan campos en barbecho y terrenos agrícolas, así como también pantanos costeros y de agua dulce. En Sudamérica, se les puede hallar en pastizales, pantanos, arrozales y granjas.[11]
En América del Norte[editar]
En el este de Estados Unidos, los campos de heno constituyen un importante hábitat reproductivo para la especie. La abundancia de charlatanes en henares viejos —de ocho años o más— en un área estudiada en Nueva York era al menos un 67% mayor a la de cualquier otro tipo de hábitat en la zona y cuatro veces superior a la de las praderas del Medio Oeste. La cantidad de charlatanes aumentaba exponencialmente con el tamaño de los henares y era mayor en aquellos campos con menor superficie cubierta por alfalfa.[33] Respecto del efecto que produce sobre las poblaciones la proximidad a los límites de los pastizales en los que anida esta especie, un estudio llevado a cabo entre 1999 y 2000 en el norte de Iowa encontró que la densidad de charlatanes era menor cerca de los márgenes de bosques que en los confines de áreas agrícolas o en las inmediaciones de carreteras y que existía una relación positiva entre la densidad poblacional de esta ave y la distancia a los tres tipos de límites estudiados.[34]
En un estudio se descubrió que los nidos ubicados a menos de 50 m de bosques y setos leñosos presentaban tasas diarias de supervivencia más bajas que aquellos situados a más de 100 m de algún tipo de límite de los pastizales en los que anidan. Los charlatanes tendían a alejarse de los márgenes de los bosques al reanidar después de que su primer intento de criar una nidada fracasara; este patrón era particularmente evidente entre las hembras que construían su primer nido dentro de los 50 m de un bosque o un seto leñoso. También evitaban nidificar en las inmediaciones de carreteras, a pesar de que las tasas de supervivencia no fueran menores en las cercanías de ese borde de hábitat. Sin embargo, no parecían eludir los límites adyacentes a antiguos terrenos agrícolas y pasturas. La supervivencia de los polluelos en las proximidades de esos tipos de bordes de hábitats era superior a la registrada cerca de los márgenes leñosos y similar o superior a la correspondiente a los nidos ubicados a 100 m o más de cualquier límite de hábitat. Las respuestas de los charlatanes a los bordes de hábitats eran inconsistentes y el éxito reproductivo dependía del tipo de borde de hábitat considerado.[35]
En América del Sur[editar]

En Sudamérica, las comunidades de hidrófitas son las de mayor importancia como hábitat para el charlatán y, por lo general, se caracterizan por la presencia excluyente de unas pocas especies de alto porte que determinan la fisonomía del lugar. En el este de la provincia de Santa Fe (Argentina), los sitios más deprimidos e inundables sustentan comunidades densas y de alto porte —mayores a 1,5 m— que son dominadas por juncos (Schoenoplectus californicus), totoras (Typha domingensis) y huajós (Thalia multiflora) y que generalmente contienen numerosas especies acuáticas arraigadas, como la saeta (Sagittaria montevidensis), o flotantes, como el repollito del agua (Pistia stratiotes). En los bordes de las comunidades anteriores y en posiciones topográficas ligeramente más elevadas se encuentran las comunidades localmente denominadas «canutillares», compuestos de gramíneas de porte bajo y mediano como Leersia hexandra y Luziola peruviana, o de canutillos de mayor porte como los del género Echinochloa; sin embargo, comúnmente no superan el metro de altura. Una mención especial merecen los espadañales, comunidades de hidrófitas en las que se destaca la especie Zizaniopsis villanensis —endémica de Argentina—, de importancia menor en la región por su escasa distribución pero de alta relevancia para el charlatán, que emplea estas comunidades como dormideros. Cabe destacar que esa espadaña pertenece a la tribu Oryzeae —la misma del arroz— y que los cultivos de este grano bien podrían representar un ambiente sustituto de los espadañales autóctonos de aquella especie; los datos históricos, de principios del siglo XX, de miles de individuos en la zona fueron previos al advenimiento de los cultivos de arroz en la región.[4] En Bolivia, se han descubierto dormideros en humedales dominados por juncos (Schoenoplectus californicus) y papiros (Cyperus papyrus), una especie introducida.[36] Una de las formaciones herbáceas de mayor importancia regional en el este de Santa Fe es el pajonal, dominado por la paja de techar (Panicum prionitis), una gramínea de alto porte que cubre extensas áreas del este santafesino. Los pajonales ocupan una posición intermedia en el gradiente topográfico y están parcialmente anegados en la estación húmeda.[4]

Las comunidades restantes son de importancia marginal para el charlatán y se ubican en posiciones de mayor altura; los árboles y arbustos constituyen sus elementos prevalentes. Las formaciones leñosas dominantes se integran con bosques xerófitos compuestos por árboles de maderas duras y semiduras de follaje caducifolio. Entre otras especies presentes en los bosques pueden mencionarse el algarrobo negro (Prosopis nigra var. ragonesei), el espinillo (Acacia caven) y el quebracho colorado chaqueño (Schinopsis balansae). En los bordes de dichas formaciones, crece con frecuencia la rama negra (Sesbania virgata), un arbusto utilizado como percha por el charlatán.[4]
Los charlatanes se adaptan fácilmente a los cambios en la distribución de los recursos alimenticios. En Trinidad (Bolivia), visitaban plantaciones de arroz en su primer año de producción en lo que había sido un área boscosa talada el año anterior, lo que sugiere que la especie es altamente móvil y sensible a los cambios en el uso de la tierra. Inversamente, en otras regiones desparecían cuando los cultivos de arroz eran reemplazados por los de soja. La especie parece mantener áreas localizadas de distribución tradicionales en zonas que han producido arroz de manera consistente, pero abandona regiones en las que otros cultivos han tomado el lugar de los arrozales. Si bien se observaron individuos alimentándose de insectos en campos de soja en ese estudio, no se halló ninguno en sojales ubicados en zonas sin producción arrocera; es probable que los charlatanes se alimenten secundariamente de insectos en cultivos de soja —téngase en cuenta que se trata de una especie principalmente granívora fuera de la temporada reproductiva— solo en regiones con arrozales y cuando los insectos son localmente abundantes.[36]
Comportamiento[editar]

Contrario a lo que sucede durante la temporada reproductiva en Estados Unidos y Canadá, en donde los charlatanes se distribuyen más uniformemente, en Sudamérica pernoctan en dormideros de decenas de miles de ejemplares en sitios anegados e inclusive en las arroceras. La denominación de «charlatán» deriva justamente de la algarabía que producen los cantos simultáneos de millares de individuos. Las bandadas suelen ser tan numerosas que por momentos ennegrecen el cielo, convirtiéndose, debido a sus movimientos alternadamente espiralados y en enjambre, en un llamativo espectáculo.[4]
Fuera de la temporada reproductiva, los charlatanes son a menudo observados junto a otras especies de ictéridos. Existen registros de charlatanes en compañía de varilleros negros (Agelasticus cyanopus), varilleros congos (Chrysomus ruficapillus), pecho amarillos chicos (Pseudoleistes virescens) e incluso ictéridos que típicamente no habitan en pantanos como el tordo músico (Agelaioides badius) y el pecho colorado (Sturnella superciliaris).[37] Los charlatanes no se alejan de sus sitios de forrajeo —cultivos de arroz o pastizales y bañados— ante la presencia de aves rapaces, sino que simplemente descienden de la parte alta de la vegetación hasta casi desaparecer al ojo del observador.[4]
Vocalizaciones[editar]

Su llamado, a menudo emitido en vuelo, ha sido descrito como un melódico pink,[38] como un inkh nasal,[22] o como un fink ascendente y jadeante.[26] También profiere un castañeteo seco.[22] Su canción, metálica y burbujeante, es un b'bob-o-lii'ink aflautado y vagamente onomatopéyico, que derivó en el nombre vulgar de la especie en inglés: bobolink.[38]
Durante la temporada reproductiva, los charlatanes machos emiten dos tipos de canciones básicos. La canción alfa comprende unas notas introductorias particulares seguidas por una serie de notas interiores y finalmente una secuencia de notas gorjeadas. La canción beta presenta sus propias notas introductorias inmediatamente sucedidas por una serie de notas gorjeadas.[39][40] Solo el 10% de las vocalizaciones articuladas por los machos son canciones alfa o beta completas, mientras que el 87% son fragmentos de canciones y el restante 3%, canciones compuestas, que constan de una canción completa de uno de los dos tipos a la que se le agregan canciones completas o fragmentadas emitidas de manera continua.[39] Mientras que la canción alfa completa dura aproximadamente 7 segundos y la beta alcanza los 4,5, las compuestas pueden superar los 20 segundos.[39][40] Debido a que el repertorio de los charlatanes incluye solo dos canciones y todos los machos cantan una versión de cada una, la posibilidad de que la amplitud de sus repertorios constituya una señal de su calidad queda excluida.[40]
No se ha encontrado evidencia de una función intersexual para una canción y una intrasexual para la otra. El comportamiento vocal de los machos territoriales antes de la llegada de las hembras a las áreas de reproducción no difiere significativamente del correspondiente al período posterior al arribo de las mismas; no es que cada tipo de canción sea más o menos usado en determinado contexto.[40] Los machos territoriales incrementan la cantidad de canciones de ambos tipos tanto en presencia de hembras como de otros machos enjaulados, en comparación a lo que sucede frente a jaulas vacías de control, y reaccionan a la presencia de individuos de su mismo sexo aumentando la proporción de canciones fragmentadas y disminuyendo la de canciones compuestas. Asimismo, incluyen menos notas por canción y emiten una mayor proporción de canciones que consistan solo en las notas introductorias en presencia de estos.[39] En un experimento en el que se dispuso machos enjaulados en los territorios de charlatanes de ese mismo sexo en presentaciones de quince minutos, alrededor de la mitad atacó al intruso mientras que la otra mitad no lo hizo; se constató que la canción proferida por el agresor antes de un ataque contenía menos notas que el promedio de las canciones de los machos no atacantes durante el período de observación.[41] En conclusión, la respuesta vocal de los machos territoriales a intrusos de su propio sexo no es más que cantar secuencias cortas y simples de cualquiera de los dos tipos de canciones.[39] Responden a la presencia de hembras con un comportamiento vocal más versátil o complejo, mientras que parecen codificar la agresión hacia sus rivales en canciones cortas, menos complejas y altamente repetitivas.[42]

Las reacciones agresivas por parte de los machos territoriales son igualmente fuertes ante ambos tipos de canciones, lo que respalda la teoría de que estas no tienen funciones específicas; frente a la reproducción de los dos tipos de canciones, los machos se acercaban a los grabadores a una distancia media de poco menos de 14 m a lo largo del período de observación y a una distancia mínima de 7,4 m. Asimismo, los machos no alteran la frecuencia con la que pasan de un tipo de canción al otro cuando se les presentan otros machos enjaulados, hembras enjauladas o jaulas vacías y tampoco lo hacen en el período posterior a la llegada de las hembras respecto del período previo; por lo tanto, es probable que el cambio entre uno y otro tipo de canción no refleje motivación alguna, ni agresiva ni sexual.[40]
Una respuesta vocal común por parte de los machos de diferentes especies paseriformes a la reproducción de canciones grabadas de congéneres de su mismo sexo consiste en que el macho se acople a la canción reproducida. Si las canciones son utilizadas en la defensa del territorio, este acoplamiento a la canción emitida por el intruso podría funcionar como una señal agresiva dirigida a un individuo en particular en circunstancias naturales. Los charlatanes machos territoriales no muestran una tendencia a acoplarse a las canciones grabadas, sino que por el contrario tienden a responder con la canción alternativa. Dado que se trata de una especie con un repertorio de solo dos canciones, esa reacción podría ser funcionalmente idéntica al acoplamiento a la canción grabada o articulada por el intruso en otras especies.[40]
Alimentación[editar]

El charlatán se alimenta de semillas, granos, insectos y arañas,[4][7] y puede representar un problema en las plantaciones de arroz.[21] Entre mayo y septiembre, los insectos comprenden el 57,1% de su dieta, siendo el 42,9% restante materia vegetal. Las orugas, los saltamontes y los escarabajos son los principales componentes de su ingesta durante el verano boreal.[30] Mientras que los insectos constituyen la mayor parte de su alimentación en su área de reproducción, estos son sustituidos por los granos de cultivo mientras migra al sur.[43] A pesar de su dieta principalmente insectívora durante la temporada reproductiva pero en consonancia con su reemplazo por los granos ya en su migración, de 215 especies neotropicales migratorias, el charlatán se encuentra entre las menos de diez que causan un daño significativo a los cultivos sobre amplias áreas geográficas en Estados Unidos.[44] Prefiere los granos de arroz verdes a los ya maduros.[4][36] Por otro lado, en sus cuarteles invernales también consume chinches, isocas y otros insectos en plantaciones de soja, girasol y sorgo.[4]
En Argentina, se alimenta fundamentalmente de semillas de pastos.[37] Consume simientes de gramíneas presentes en las arroceras y consideradas malezas por los productores de arroz. Las semillas del gramillón o pasto de bañado (Echinochloa polystachya), una gramínea abundante en paisajes inundados, representan una importante fuente de alimento para el charlatán en Sudamérica; no obstante, las praderas «puras» de esta planta podrían no ser el mejor hábitat para su alimentación por la falta de estructuras vegetales firmes que sostengan a las aves evitando que estas caigan al agua, pero, en combinación con otras especies como la escoba dura (Vernonia incana) y las onagras (Oenothera sp.), sobre las cuales se posan los charlatanes para alcanzar las simientes de gramillón, el hábitat es idóneo y su oferta en período de inundación, ilimitada.[4] Otras especies cuyas semillas ingiere el charlatán en Sudamérica incluyen Brachiaria sp.,[36] Echinochloa crus-galli,[36] Leptochloa filiformis,[36] Leptochloa virgata,[36] Paspalum intermedium,[37] Paspalum urvillei,[37] Paspalum virgatum,[36] Schoenoplectus californicus,[37] Sorghum arundinaceum[36] y Sorghum halepense.[37] Los dientes de león (Taraxacum officinale) constituían la principal fuente de simientes consumidas por los machos adultos en mayo en el sudeste de Oregón,[30][45] en donde infrecuentemente comían gusanos cortadores y otros insectos. Otras plantas de cuyas semillas se alimentan en junio en ese estado son Achillea millefolium, Cirsium arvense, Malva moschata, Potentilla glometrata, Rumex crispus y Thermopsis montana.[30]
Su manera de procurarse el alimento consiste en alcanzar las simientes arqueando las espigas con su propio peso y/o utilizando atalayas a la misma altura de las semillas entre el pastizal. Persiguen a los artrópodos por debajo y entre las hojas, por ejemplo de girasol o de soja, recorriendo mayormente la parte media de los cultivos.[4] Si bien se alimenta típicamente durante el día, se le ha observado hacerlo en noches claras en arrozales cuando intenta almacenar reservas de grasa para su viaje a través del mar.[7]
Reproducción[editar]

La mayoría de los machos llega a las áreas de reproducción en América del Norte y pronto establece sus territorios entre mediados y fines de mayo; las hembras arriban a fines de mayo y comienzos de junio.[30] En el sudeste de Oregón, las hembras escogen compañero entre aproximadamente el 20 de mayo y el 10 de junio y los nidos albergan polluelos desde alrededor del 11 de junio hasta el 7 de julio.[46] Esta especie cría normalmente una sola nidada por año,[31][32][46][47] aunque las hembras pueden volver a anidar si su primer intento de criar una nidada fracasa.[27] Ocasionalmente, es víctima del parasitismo de puesta por parte del tordo cabecicafé (Molothrus ater), un ictérido cuya reproducción requiere la puesta de sus huevos en los nidos de otras aves.[48][49] En un estudio en henares de Nueva York en el que se siguió la evolución de 33 nidos de charlatán, cada pareja produjo un promedio de tan solo 0,3 polluelos que lograran abandonar el nido; mientras que el 85% de los nidos resultó improductivo debido a las prácticas agrícolas, otro 9% lo fue por causa de la depredación.[44]
Filopatría[editar]

Los charlatanes —especialmente los machos— demuestran conductas filopátricas, es decir, tienden a regresar a las mismas áreas de reproducción año tras año.[12][50] Sin embargo, el éxito en la crianza de los polluelos en una determinada temporada influye en la elección del sitio reproductivo del año siguiente en ambos sexos.[50] Las hembras cuyas crías no hayan sobrevivido en cierto lugar no son proclives a volver allí.[12] De manera similar, existe evidencia que indica que, entre los machos de cuyos nidos logra independizarse al menos un polluelo, aquellos que regresan a las mismas áreas a aparearse suelen haber tenido un éxito reproductivo sensiblemente superior el año anterior que los que no lo hacen. En los territorios de los machos fieles a los sitios de procreación, se construyen más nidos, se depositan más huevos, eclosiona un mayor número de estos y más polluelos logran abandonar el nido que en los dominios de aquellos que no vuelven en años subsecuentes. Asimismo, para las hembras filopátricas es mayor el número de huevos que eclosiona y de polluelos que abandona el nido tanto en términos absolutos como por huevo depositado, en comparación a las hembras que no regresan.[50]

Los charlatanes en sitios reproductivos buenos logran criar hasta su independencia a una cantidad significativamente superior de polluelos y muestran una tendencia considerablemente mayor a la filopatría que los que anidan en sitios reproductivos pobres. Mientras que los reproductores exitosos —aquellos que lograron criar satisfactoriamente al menos a uno de sus polluelos el año previo— exhiben la misma propensión a volver a sitios reproductivos de cualquier calidad, los reproductores no exitosos en sitios favorables son más de tres veces más proclives a regresar que aquellos en sitios menos propicios. La tasa de retorno no difiere entre las aves que hayan tenido éxito en la cría de sus pequeños y las que no en sitios fecundos, pero en los de baja calidad aquellas que no lograron dejar descendencia son mucho menos propensas a volver que las que sí lo lograron. Los charlatanes que regresan a los sitios pobres a pesar de no haber conseguido criar a sus polluelos el año anterior tienden a establecerse en un lugar más alejado del que escogieron la temporada previa respecto del que eligen los reproductores exitosos; esto contrasta con lo ocurrido en sitios de alta calidad, en los que la distribución de los individuos filopátricos no difiere según la suerte que hayan corrido sus nidadas el año anterior. Las hembras —no así los machos— que se reprodujeron en un determinado sitio en uno o más años previos son más propensas a volver que aquellas que anidan allí por primera vez. Las aves cuyos nidos son destruidos por la cosecha del heno muestran una tasa de retorno similar a la de los reproductores no exitosos por causas naturales. Los patrones de comportamiento filopátrico en el charlatán son primordialmente resultado de elecciones basadas en la experiencia y no constituyen un mero reflejo de los patrones de mortalidad.[51]
Territorio y cortejo[editar]

En el noroeste de Pensilvania, los machos llegan a las áreas de reproducción a fines de abril o a principios de mayo. Varios días después de su arribo y antes de que lleguen las hembras, los machos comienzan a establecer sus territorios. Las hembras arriban aproximadamente entre siete y diez días después que los machos.[40] La propiedad territorial está generalmente bien establecida para la segunda semana tras la llegada de aquellos.[39] Los territorios tienen una extensión de entre 0,5 y 1,25 hectáreas.[40]
El macho corteja a la hembra en una postura también adoptada por otros ictéridos: la cabeza baja, las plumas del cuello infladas, la cola desplegada y las alas arqueadas hacia abajo, exhibiendo las notorias manchas blancas en sus hombros.[38] Las exhibiciones en vuelo de los charlatanes machos consisten en una serie de rápidos batimientos de las alas intercalados con cortos planeos a alturas variables entre los 2 y los 40 m sobre sus territorios. Las batimientos alares son más veloces que en el vuelo ordinario. Cada exhibición puede durar de unos pocos segundos a alrededor de un minuto. Durante el período de cortejo, los machos pasan aproximadamente el 10% del día exhibiéndose en el aire. La duración estas exhibiciones energéticamente costosas está positivamente relacionada con la condición física de los machos y con la cantidad de polluelos que lograrán criar exitosamente.[52]
Poliginia[editar]

Los machos son con frecuencia poligínicos,[18] con hasta cuatro hembras anidando simultáneamente en sus territorios.[21][31][32] En diferentes poblaciones, se han determinado porcentajes del 25%[32] y del 55% de machos poligínicos.[53] Este tipo de emparejamiento es sucesivo, no simultáneo: un macho nunca adquiere una segunda hembra dentro de los tres días de haber conseguido la primera.[25]
Es probable que los machos con más de una compañera sean mayores y más experimentados y que, por lo tanto, puedan reclamar mejores territorios.[21] Dentro del Malheur National Wildlife Refuge, en el sudeste de Oregón, se constató que el área que parecía constituir el hábitat más apropiado para que los charlatanes se establecieran contenía los espacios ocupados cada primavera en primer lugar tanto por machos como por hembras, los territorios más pequeños en promedio, la mayor frecuencia de emparejamientos poligínicos y la menor proporción de machos sin pareja.[25] Sin embargo, en el valle del río Pend Oreille, en el extremo noreste de Washington, se encontró que eran los territorios de los machos monógamos los que, aunque algo más pequeños, presentaban la mayor densidad de orugas y la cubierta herbácea más alta.[53]

Las hembras arribaron a esa área de estudio en tres oleadas con una superposición mínima entre ellas. Las primeras en llegar elegían los territorios pequeños y establecían vínculos de monogamia con sus compañeros: aunque predeciblemente los primeros machos en conseguir pareja ostentaban los territorios de mayor calidad, se observó que estos territorios correspondían a machos monógamos, lo cual contrasta con la teoría que sostiene que los primeros territorios ocupados por las hembras, por ser más favorables, deberían pertenecer a eventuales machos poligínicos. Las que arribaban luego escogían los territorios restantes, más extensos, y la mayoría de ellas se convertía en las compañeras primarias de algún macho poligínico. Las que llegaban por último se emparejaban poligínicamente en esos grandes territorios y devenían las compañeras secundarias de los propietarios de dichas parcelas. El tardío y, en su mayoría, monógamo establecimiento de las hembras en territorios próximos a densas arboledas de álamos balsámicos de California (Populus trichocarpa) se debe a que las extensiones cubiertas por árboles inhiben la nidificación del charlatán. Mientras que las hembras monógamas lograban criar una mayor cantidad de polluelos hasta que abandonaran el nido, entre los machos esto se daba en los poligínicos.[53]
Los machos poligínicos dedican la mayor parte de su tiempo y atención a la primera compañera que hayan conseguido en la temporada y a sus polluelos, asistiendo en la alimentación y la defensa de los pequeños en los nidos de otras hembras solo cuando el tiempo y los recursos lo permiten.[21] Según estudios llevados a cabo por Martin en Wisconsin, los machos poligínicos alimentan casi exclusivamente a los polluelos primarios —es decir, aquellos de su primera compañera— y solo rara vez proporcionan alimento a los secundarios.[12][46] Consecuentemente, la descendencia de las hembras secundarias está más expuesta a la desnutrición y puede experimentar una tasa de mortalidad más elevada.[12][25][46] Por otro lado, en el sudeste de Oregón, Wittenberger encontró que los machos poligínicos aprovisionaban regularmente tanto los nidos primarios como los secundarios.[46]
Adaptaciones de las hembras secundarias[editar]

Las hembras secundarias han desarrollado diversas adaptaciones para hacer frente a la reducida asistencia del macho en sus nidos. Por empezar, sus puestas son menos numerosas que la de la principal. El hecho de que la incubación comience tras la puesta del penúltimo huevo asegura una eclosión asincrónica de los mismos; en tiempos de escasez de comida, el polluelo que haya eclosionado más tarde puede pasar hambre y ser aniquilado para evitar poner en riesgo la nidada entera. Asimismo, las hembras secundarias muestran una mayor tendencia a sacar provecho de los insectos que hallen en las cercanías del nido, dentro de los 60 m de este, y son menos selectivas en cuanto al alimento. La asistencia parcial del macho en casos en los que las nidadas secundarias son excepcionalmente numerosas también es importante, contribuyendo a optimizar el desempeño reproductivo de las aves emparejadas poligínicamente.[12]
Nidadas reducidas[editar]
Una combinación de tres factores contribuye potencialmente a que las puestas de las hembras secundarias sean de menor tamaño. Uno de ellos es su edad fisiológica. Las primeras en llegar a las áreas de reproducción —y, por ende, las que se convierten en las compañeras principales de los machos poligínicos— tienen al menos 2 años de edad. Un estudio que siguió a 7 hembras nacidas el mismo año demostró que en su primera aparición como ejemplares sexualmente maduros estas tardaron entre 1,5 y 2 semanas más que las aves de 2 años o mayores en alcanzar las áreas de reproducción y, en consecuencia, las 7 se convirtieron en compañeras secundarias de algún macho. Existe evidencia de que el número de huevos depositados aumenta con la edad: esas mismas 7 hembras pusieron un promedio de 3,8 huevos en su primer año, 5,6 huevos en el segundo, 5,7 huevos en el tercero y 5,9 huevos en el cuarto. En conclusión, las hembras de mayor edad tienden a ser las compañeras principales de los machos y a tener nidadas más numerosas que las jóvenes, las cuales adquieren un estatus secundario debido a su tardío arribo a las áreas de reproducción. Es probable que una puesta reducida mitigue el estrés en hembras inexpertas en el cuidado de los polluelos.[12]

La renidificación es el segundo factor que estaría involucrado en el menor tamaño de las nidadas secundarias. Cuando el nido de una hembra es destruido, en ocasiones esta permanece en la zona para construir uno nuevo. La segunda puesta siempre es uno o dos huevos más pequeña que la original. En estos casos, generalmente se emparejan con un macho en una relación secundaria. Cada año, después de las cosechas tempranas de la alfalfa, un cierto número de hembras con placas de incubación bien desarrolladas y vascularizadas —evidencia de una puesta reciente— aparece en los prados cercanos para volver a anidar.[12]
Por último, existe la posibilidad de una adaptación psicológica de las hembras con respecto a su estatus. Aunque las compañeras de un mismo charlatán no muestran un comportamiento de abierta animosidad entre ellas —como sí lo hacen las de tordo sargento (Agelaius phoeniceus) y tordo cabeciamarillo (Xanthocephalus xanthocephalus)—, las hembras principales a veces exhiben conductas agresivas hacia las secundarias, haciendo que estas posiblemente tomen conciencia de su condición antes de la puesta de los huevos. Hembras que han depositado siete huevos como compañeras primarias de algún macho en una o dos temporadas anteriores pueden reducir sus nidadas a cinco o seis en otro año tras la desaparición de sus compañeros —a pesar de haber sido las hembras primarias de estos también en este último año—, en cuyo caso pueden aparearse luego con otros machos y aun así no recibir ayuda en el cuidado de los polluelos; en la temporada siguiente, nuevamente como hembras principales y con la presencia de sus compañeros después del período de cópula, pueden volver a poner siete huevos. Estas observaciones sugieren que un estímulo derivado de ciertas relaciones intraespecíficas —o bien, de la falta de algunas interacciones— podría influir en la cantidad de huevos depositados, lo cual constituiría una importante adaptación pues estas hembras afrontarían quizá grandes dificultades si debieran criar a siete polluelos sin la asistencia de un macho.[12]
Eclosión asincrónica[editar]

Existe considerable evidencia de que la eclosión asincrónica o la matanza selectiva de parte de la nidada en favor del resto de la misma son comunes en algunas especies poligínicas, tales como el tordo tricolor (Agelaius tricolor), el chivirín pantanero (Cistothorus palustris), el tordo cabeciamarillo (Xanthocephalus xanthocephalus) y el tordo sargento (Agelaius phoeniceus).[12] En el charlatán, la incubación comienza tras la puesta del penúltimo huevo.[12][31] Esto resulta en una eclosión asincrónica de los polluelos, lo que implica que uno de ellos nacerá aproximadamente veinte o treinta horas después de sus hermanos. Si una hembra no pudiera mantener un suministro adecuado de alimentos, el más joven del nido rápidamente sufriría la falta de comida y sería eliminado antes de que se desperdiciara alimento en un vano intento de salvar su vida. Esto incrementaría la inversión relativa de la hembra con respecto a la supervivencia de sus polluelos y aplacaría el riesgo de una intensa competencia entre los hermanos. Entre 1967 y 1972 en Wisconsin, este fenómeno representó la muerte de un promedio de 0,99 polluelos por nido secundario —entre 0 y 3, considerando los casos estudiados por separado— y de 0,26 polluelos por nido principal —de 0 a 2 en casos particulares—. Debido a las diferencias iniciales en el tamaño de las nidadas y las muertes resultantes de la eclosión asincrónica, los nidos secundarios contenían un promedio de 1,4 polluelos menos que los principales: 5,2 y 3,8 respectivamente. Esta característica de su biología reproductiva también se aplica a las hembras primarias bajo circunstancias desfavorables en las que la muerte de un polluelo garantiza la supervivencia del resto.[12]
En los años en los que hay una abundancia excepcional de alimento o condiciones climáticas benignas que permitan a las hembras secundarias embarcarse en expediciones más prolongadas en busca de comida, todos los jóvenes tienen más posibilidades de estar debidamente nutridos. En estos casos, los polluelos más grandes se sacian, dando oportunidad a los más pequeños de obtener alimento.[12]
La suma de puestas menos numerosas y eclosión asincrónica aseguran a las hembras secundarias un éxito reproductivo variable, sensible a la disponibilidad de comida. En condiciones apropiadas, la reducción de la nidada no es necesaria y las hembras sin ayuda de un macho son capaces de criar a todos sus polluelos. Cuando el alimento es insuficiente para cubrir satisfactoriamente las demandas de su descendencia, el último en romper el cascarón es rápida y eficientemente removido del nido. Frente a tales circunstancias, sin embargo, las nidadas grandes requieren la eliminación de dos polluelos, uno de los cuales habrá eclosionado simultáneamente con la mayor parte de sus hermanos y consumiría una ración de comida que sería mejor invertida si se repartiera entre unos pocos sobrevivientes, pudiendo debilitar a todos ellos. Consecuentemente, si bien la reducción de la nidada puede ser un recurso importante para circunscribir la cantidad ya disminuida de polluelos en un nido, funciona óptimamente solo cuando el tamaño de la puesta de una hembra secundaria se adecua con precisión a los suministros promedio de alimento de estos nidos.[12]
Flexibilidad en la atención por parte del macho[editar]

Según las observaciones de Martin (1974) —que difieren de las Wittenberger (1980)—, los machos no colaboran con sus compañeras secundarias en la crianza de los polluelos como regla general. No obstante, en casos en los que las puestas secundarias son inusualmente numerosas —5 o 6 huevos—, el macho divide su tiempo de manera desigual entre los jóvenes de la hembra primaria y los de las secundarias, concentrándose en los primeros, algunos días mayores. La asistencia de este en los nidos secundarios no suele darse sino hasta los 4 o 5 días de haber nacido los polluelos y es frecuentemente precedida por la reducción de la nidada. En esta instancia en la que las hembras se encuentran severamente sobreexigidas, la ayuda de su compañero indudablemente contribuye a la crianza de juveniles más sanos y fuertes y probablemente reduce el estrés en aquellas.[12]
Esto fue demostrado en un experimento en el que 6 polluelos de 3 días de edad fueron añadidos a 4 polluelos de 3 días en un nido secundario que hasta ese momento había sido ignorado por el macho, que se había estado ocupando de la alimentación de los 7 polluelos de 8 días de edad en el nido principal. Dentro de las dos horas de comenzado el experimento, el macho empezó a llevar comida al nido secundario, mientras aún dirigía la mayor parte de su atención a los hijos de la hembra principal. Dentro de los tres días, este nido secundario devino el centro de atención de aquel. Tres de los polluelos murieron en el nido superpoblado, pero los otros 7 lograron abandonarlo gracias a la cooperación de ambos adultos. Esto quiere decir que los machos atienden a sus compañeras secundarias cuando estas tienen demasiado trabajo; pueden advertir las ocasiones en las que la crianza de una nidada excede la capacidad de un solo progenitor. En caso de depredación o pérdida del nido principal, los machos redirigen su esmero al nido secundario cuyos polluelos hayan eclosionado antes.[12] Sin embargo, a diferencia de lo sucedido entre los tordos cabeciamarillos (Xanthocephalus xanthocephalus) poligínicos en experimentos, es poco usual que un charlatán macho redirija sus cuidados paternales a un nido secundario tras la reducción natural de su nidada primaria.[46]
Sobre el final de la temporada de reproducción, después de que los hijos de la hembra principal se hayan independizado, algunos machos comienzan a alimentar a los de la secundaria. Puede ser una adaptación por parte de las hembras secundarias el relegar la nidificación hasta un momento que minimice el período de superposición de dependencia de los polluelos primarios y los propios con respecto a sus padres. De este modo, los machos colaboran más frecuentemente con las hembras secundarias, cuyas nidadas pueden ser entonces de mayor tamaño. Este comportamiento reproductivo ha sido identificado también en el chivirín pantanero (Cistothorus palustris); sin embargo, una posposición demasiado prolongada no es viable en los charlatanes debido a lo abreviado de su temporada de reproducción. En esta especie, pasan entre 45 y 50 días desde que los adultos encuentran pareja hasta que los polluelos se independizan de sus padres, y los jóvenes deben convertirse en fuertes voladores antes de su migración al sur.[12]
Resultado de las adaptaciones a la poliginia[editar]
El menor tamaño de las nidadas secundarias, la eclosión asincrónica, la gran regularidad con la que estas hembras alimentan a sus polluelos a pesar de no ser usualmente ayudadas por el macho y la plasticidad en los patrones de crianza por parte de este evidenciada bajo circunstancias inusuales que requieren su asistencia en dichos nidos, constituyen una serie de importantes adaptaciones que impide un fracaso reproductivo masivo en las hembras secundarias. Esto, combinado con una flexibilidad en el sistema de emparejamiento que asegura que todas las hembras tengan la posibilidad de reproducirse en un hábitat donde las condiciones provean una oportunidad razonable de éxito, favorece la poliginia como estrategia reproductiva en ecosistemas en los que el alimento se encuentra generalmente concentrado.[12]
Nido y huevos[editar]

Los charlatanes anidan en colonias pequeñas y algo disgregadas. La hembra remueve la vegetación para crear un espacio libre sobre el suelo en el que excava una pequeña depresión para el nido.[24] Este presenta forma de taza[4][18][32] y consiste en una pared externa de césped seco y tallos de hierbas con un recubrimiento interno de césped más fino y ciperáceas;[7][21] las fibras son entretejidas con soltura.[24] El nido suele estar bien oculto en sitios en donde la hierba es densa y alta.[11][18] La hembra deposita en él 5 o 6 huevos[43][18] —ocasionalmente, entre 1 y 7—[4] de un color gris azulado o marrón rojizo pálido con manchas irregulares oscuras,[4][7] de 20,5 - 23,4 mm de largo por 15,1 - 17,3 mm de ancho.[7] Pone un huevo por día y da inicio a la incubación con la puesta del penúltimo huevo.[12][31] El período de incubación varía entre los 11 y los 13 días.[4][7][24] En el sudeste de Oregón, el intervalo promedio entre la eclosión de los polluelos primarios y la de los secundarios fue de 6,0 días en 1973, 4,4 días en 1974, 3,8 días en 1975 y 7,2 días en 1976.[46]
A lo largo de su área de distribución reproductiva rara vez el tordo cabecicafé (Molothrus ater) deposita sus huevos en nidos de charlatanes.[49] Sin embargo, en un estudio llevado a cabo entre 1996 y 1999 en Dakota del Norte, 11 de 36 nidos de esta especie contenían huevos del parásito, lo que equivale a una incidencia parasítica de un 30,6%.[54] En ocasiones, los charlatanes persiguen y picotean a los tordos cabecicafé o emiten llamados de alarma en presencia de estos.[54][55] Los polluelos pueden sufrir la depredación de la grulla canadiense (Grus canadensis).[46]
Crianza de los polluelos[editar]

Ambos progenitores participan de la alimentación de la nidada[18][31][32] y aprovisionan a los polluelos con progresiva frecuencia a medida que estos crecen.[25] Los polluelos son altriciales y adquieren la capacidad de volar entre 10 y 14 días después de haber nacido.[4][7] El principal alimento dado a los pequeños son las larvas de lepidópteros —entre las que se destacan las orugas de árctidos y noctúidos— y de avispas de sierra.[46][25] También son alimentados con saltamontes, lepidópteros adultos —como Cisseps fulvicollis—, coleópteros, dípteros, pupas de lepidópteros, arácnidos, hemípteros, himenópteros adultos, neurópteros, efemerópteros, odonatos y anélidos. Los machos capturan orugas y saltamontes significativamente más grandes que las hembras.[25]
Los polluelos comienzan a pedir alimento pocos minutos después de romper el cascarón. Durante los primeros días tras su eclosión, el macho y la hembra principal a menudo intercambian roles: mientras uno se queda dando calor a la nidada, el otro va en busca de comida, pudiéndose alejar 400 o 500 m del nido. Esto les permite además seleccionar alimentos más grandes y nutritivos para traer de regreso. Así, los pequeños disponen de alimento y de una temperatura adecuada de manera más o menos continua. En las mañanas frías, las hembras secundarias, en cambio, solo pueden abandonar el nido por lapsos reducidos. Por esta razón, es probable que sus polluelos reciban menos comida en un principio.[12] En términos generales, sin embargo, Martin (1974) encontró que la cantidad de alimento dada a los polluelos por parte de una hembra secundaria durante el proceso de crianza no era muy inferior a las cantidades conjuntas del macho y la hembra principal en el nido de esta, estableciéndose cierto equilibrio.[25][12] No obstante, el hecho de que el tamaño de las nidadas secundarias promediara solo el 70% del de las primarias en la muestra tomada por Martin fue motivo al menos parcial de esta percibida respuesta compensatoria por parte de las hembras secundarias en referencia a la alimentación por polluelo considerado individualmente. Wittenberger (1982) descubrió que en el sudeste de Oregón, en donde las nidadas secundarias generalmente no eran más chicas que las primarias, las hembras secundarias no compensaban la reducida asistencia masculina incrementando la cantidad de alimento que ellas proporcionaban a sus polluelos, excepto en uno de los cuatro años que duró el estudio en el que la comida abundaba y las condiciones meteorológicas eran favorables. El costo para una hembra de aceptar el estatus de compañera secundaria era sustancial debido a que los machos son menos propensos a contribuir con la alimentación de los polluelos en nidos secundarios cuando estos son aún pequeños, momento en el que su ayuda es especialmente importante, y porque son menos proclives a colaborar en absoluto bajo condiciones de escasez de alimento y mal tiempo.[25]

Las hembras y los machos adaptan la cantidad de tiempo que pasan empollando y alimentando a los polluelos en los nidos primarios de acuerdo a las condiciones meteorológicas predominantes y a la disponibilidad de alimento. Las hembras primarias los empollan más y mantienen los niveles de alimentación cuando la comida es escasa y el tiempo es tormentoso. Cuando el alimento escasea y el tiempo es bueno, las hembras primarias los empollan menos y los alimentan más. Bajo estas condiciones, según se observó, las hembras llevaban comida a los polluelos de 10 días con mayor frecuencia, les entregaban una cantidad más elevada de presas por viaje a los de entre 7 y 10 días, suministraban una mayor biomasa por hora a los polluelos de esa misma edad y pasaban menos tiempo atendiendo a los polluelos de entre 4 y 10 días que en otras circunstancias.[25]
Los machos empollan menos a los polluelos y los alimentan más —mayor frecuencia en la alimentación, cantidad de presas por viaje y biomasa suministrada por hora— cuando el alimento escasea, sin importar las condiciones meteorológicas. La medida en la que los machos alimentan a los polluelos se ajusta a la condición nutricional de los mismos y por lo tanto varía de acuerdo a la capacidad de las hembras de alimentarlos; esta conclusión es respaldada por el descubrimiento de que los machos aportan la mayor proporción de alimento a los polluelos durante el período en que aún deben ser empollados y cuando la comida es escasa y el tiempo, adverso. Inversamente, la menor contribución de los machos se produce cuando el alimento abunda y las condiciones meteorológicas son buenas. Los machos proporcionaron alrededor del 60% del alimento entregado a los polluelos primarios cuando las condiciones meteorológicas eran adversas y la disponibilidad de alimento era reducida, aproximadamente el 50% cuando el tiempo era favorable y la comida escaseaba y cerca del 40% cuando las condiciones meteorológicas eran buenas y la comida abundaba.[25]

En los nidos primarios, la atención brindada —entendida como el tiempo que los adultos pasaban en estos empollando o alimentando los polluelos, representando la primera actividad un mayor proporción de tiempo— variaba en pequeña medida a lo largo del día.
Los requerimientos de alimento de los polluelos son mayores temprano en la mañana y justo antes de que oscurezca puesto que deben sobrevivir a la noche a partir de sus reservas de grasa; por esa razón son alimentados más rápido y empollados menos tiempo en esos momentos del día. La necesidad de ser empollados y alimentados parece reducirse al mínimo cerca del mediodía, momento en el cual las hembras probablemente pasen más tiempo alimentándose. Sin embargo, bajo condiciones atmosféricas desfavorables, los requerimientos de calor permanecen altos durante todo el día.[25]

En los nidos primarios, la tasa de incremento diario en la frecuencia de la alimentación de los polluelos varió significativamente entre el 4,5% y el 15,5% por parte de los machos en distintos años según las condiciones meteorológicas y la abundancia de alimento y se mantuvo a niveles estables que oscilaron entre el 9,4% y el 14,2% para las hembras. En cuanto a los nidos secundarios, la alimentación por individuo de los polluelos por parte de las hembras fue significativamente más sustancial que en los primarios en 1973 y 1976 —debido a una mayor frecuencia en la alimentación en el primer caso y a causa de nidadas en promedio más pequeñas en el segundo—, pero no en 1974 y 1975.[25]
La frecuencia en la alimentación por cada polluelo de entre 7 y 10 días tomado individualmente no estaba negativamente relacionada con el tamaño de la nidada en 1973 y 1974, cuando el alimento era abundante. Sin embargo, esta decrecía significativamente con un mayor tamaño de la nidada en polluelos de entre 2 y 5 días, principalmente debido a una menor involucración del macho en su alimentación. Quizá los polluelos de menos edad en nidadas grandes necesitaran un suministro de energía más reducido debido a que la proporción entre volumen y superficie y, por lo tanto, la pérdida de calor son inferiores en esos nidos. En 1975 y 1976, cuando el alimento fue escaso, la frecuencia en la alimentación por individuo disminuía con un creciente tamaño de la nidada tanto para los polluelos jóvenes como para los mayores.[25]
No es evidente ninguna relación entre la edad de los polluelos primarios y secundarios y el inicio de la colaboración del macho en su cuidado.[25][46] Los machos continúan alimentando a los polluelos primarios después de comenzar a aprovisionar a los secundarios. La condición nutricional de los polluelos primarios es importante a la hora de determinar de qué manera los machos poligínicos distribuyen su esfuerzo en el cuidado de los pequeños. En los años en los que los polluelos primarios abandonan el nido con pesos elevados y no abren sus picos muy efusivamente al acercarse el investigador al nido —ambas, señales de un buen estado nutricional—, los machos poligínicos comienzan a alimentar a los polluelos secundarios pasados menos días desde su nacimiento.[46]
El comportamiento de los machos poligínicos justo antes de alimentar a los polluelos secundarios sugiere que aquellos podrían estar respondiendo directamente al estado de los polluelos primarios. Antes de aprovisionar a los nidos secundarios, los machos poligínicos casi invariablemente se posan primero cerca de sus nidos principales y dirigen sus cabezas hacia abajo, aparentemente para escuchar los agudos chillidos de sus polluelos. Solo después vuelan a los nidos secundarios y alimentan a sus pequeños allí, aunque otras veces se agachan y dan de comer a los primarios. Ocasionalmente, los machos exhiben un comportamiento similar antes de ir en busca de alimento, posándose primero cerca de su nido principal y luego, del secundario, bajando su cabeza en cada oportunidad. Tras volver con comida, generalmente repiten la secuencia antes de alimentar a los polluelos secundarios. En un caso extremo, un macho voló de su nido primario al secundario ida y vuelta cuatro veces, posándose y bajando su cabeza en cada ocasión, antes de finalmente alimentar a sus polluelos secundarios.[46]
A veces, más de dos charlatanes alimentan a los jóvenes de un solo nido. Este fenómeno, conocido como reproducción cooperativa, es poco frecuente entre migradores de largas distancias. Puede encargarse de la tarea un adulto extra de cualquier sexo. Existen diversas explicaciones para este comportamiento. Los análisis genéticos sugieren que en el caso de que el adulto extra sea un macho, tanto este como el compañero de la hembra pudieron haber concebido a uno o más de los polluelos en el nido. Puesto que esta especie muestra una marcada tendencia a regresar a las áreas en donde lograron criar a sus pequeños exitosamente o a donde ellos mismos fueron criados, los colaboradores pueden ser hijos de uno de los otros adultos o de ambos, nacidos el año anterior. Otra posibilidad es que sean individuos sin ninguna relación de parentesco cuyos polluelos no hayan sobrevivido pero que aún conserven la necesidad biológica de alimentar a los jóvenes.[21]
Cópulas y fecundaciones fuera de la pareja[editar]
Se constata en esta especie una estrategia reproductiva mixta: los machos forman vínculos de pareja con una o más compañeras para asegurar el cuidado de los nidos, pero al mismo tiempo los individuos de ambos sexos copulan con otros charlatanes. Los resultados de un estudio llevado a cabo en Nueva York centro-occidental entre 1983 y 1986 sugerían que un estimado de un 14,6% de los polluelos había sido concebido por un macho distinto del compañero de sus madres y que el 38% de los nidos contenía al menos un polluelo engendrado de esta manera por algún macho que no fuera su padre putativo. Por otro lado, a diferencia de lo que sucede con muchas aves que se reproducen en colonias, no se detectaron casos de parasitismo de puesta intraespecífico, lo que, en contraste con el caso de los machos, permite calcular con exactitud el éxito reproductivo de cada hembra contando la cantidad de polluelos que lograron independizarse de sus nidos. Las cópulas fuera de las parejas no parecían estar relacionadas con la densidad poblacional.[32]
Los machos jóvenes y las hembras mayores son más proclives a tener en sus nidos polluelos no concebidos en cópulas entre la pareja que los machos mayores y las hembras jóvenes. La frecuencia de presencia de polluelos ilegítimos en nidos de machos novicios —aquellos no detectados en años anteriores en los sitios de estudio y, dada la marcada tendencia a la filopatría en esta especie, presumiblemente más jóvenes—, estimada en un 36% de los polluelos en sus nidos, era más de tres veces superior a la correspondiente a machos marcados en temporadas previas (10%). Respecto de los nidos tomados en su conjunto, la proporción de tres a uno se repetía: se calculó que el 77% de los nidos de machos novicios contenía al menos un polluelo que no fuera hijo suyo, en comparación a un 25% entre los machos filopátricos. Es posible que estas diferencias se deban a que los machos de mayor edad estén más alerta y sean más efectivos en la defensa de sus compañeras y a que las hembras emparejadas con machos maduros probablemente sean menos propensas a copular con otros machos debido a la alta calidad de sus compañeros. Por otro lado, la proporción estimada de polluelos engendrados por un macho distinto de su compañero en nidos de hembras novicias (11%) era solo la mitad de la encontrada en nidos de hembras identificadas épocas reproductivas anteriores (22%). Las tasas estimadas de fertilizaciones ajenas a la pareja eran más elevadas cuando machos novicios se emparejaban con hembras experimentadas (39% de los polluelos) y más bajas cuando machos marcados en años anteriores formaban pareja con hembras novicias (2%). Los otros dos tipos de parejas presentaban tasas intermedias.[32]
Respecto del estatus de las hembras, las compañeras primarias de machos poligínicos eran más propensas a tener hijos con otros machos (24% de sus polluelos) que las secundarias (4%); las monógamas presentaban tasas intermedias (12%). Los polluelos resultantes de estas cópulas fuera de la pareja no eran significativamente más habituales en nidos de machos poligínicos (16%) que en los de machos monógamos (15%). Los machos responsables de las fertilizaciones fuera de la pareja parecían ser machos territoriales —incluyendo aquellos que a pesar de haber reclamado un territorio no habían conseguido ninguna compañera— y no transeúntes y por lo general tenían sus territorios cerca de los de los machos «engañados». En el 71% de los casos, el propietario de algún territorio adyacente al del macho engañado exhibía el genotipo apropiado como para haber engendrado los polluelos ilegítimos. Ese porcentaje ascendía al 95% si se consideraban los machos en un radio de dos territorios desde el del macho engañado.[32]
Las observaciones sugieren que no solo los machos sino también las hembras buscaban activamente copular con individuos distintos de sus compañeros. En varias ocasiones, se descubrieron hembras en compañía de algún otro macho en el territorio de este durante los períodos de construcción del nido o puesta de los huevos de aquellas. Las hembras también parecían intentar suscitar persecuciones por parte de múltiples machos justo antes de ese período al emitir vocalizaciones agudas. Asimismo, los machos bígamos parecían estar involucrados en más fertilizaciones fuera de la pareja que los monógamos de lo que se esperaría por casualidad; quizá estos machos hayan sido más solicitados por las hembras debido a su superioridad genética.[32]
Sin embargo, también cabe la posibilidad de que las cópulas fuera de la pareja no hayan sido favorecidas por las hembras sino que hayan resultado principalmente de patrones de comportamiento masculino. Por ejemplo, los machos podrían haber tenido más interés en copular con hembras mayores dado que su éxito reproductivo anual promedio es superior al de las jóvenes. Además, el hecho de que los nidos de las compañeras primarias de los machos poligínicos presentaran la tasa más alta de polluelos ilegítimos parece guardar mayor consonancia con la hipótesis de la persecución masculina que con la de la solicitación femenina. Ocupados en la tarea de procurar atraer más hembras, los machos podrían haber sido menos efectivos en la defensa de sus compañeras primarias, lo que posiblemente haya llevado a los altos niveles de infidelidad registrados por parte de estas; de manera similar, las escasas posibilidades de conseguir otras hembras para cuando sus compañeras secundarias se establecían y la probablemente mayor efectividad de su defensa de estas hembras podrían explicar la reducida proporción de plolluelos ilegítimos en esos nidos. Por último, los machos territoriales que no consiguieron compañeras parecían engendrar polluelos a tasas equivalentes a su proporción dentro de la población. Resulta poco probable que las hembras estuvieran interesadas en copular con ellos. Sin embargo, como estos no tenían compañeras eran libres de dedicar todo su tiempo a buscar hembras ajenas con las que copular.[32]
Las tasas de fertilizaciones derivadas de cópulas fuera de la pareja entre los charlatanes son intermedias respecto de los porcentajes obtenidos para otras especies de aves estudiadas, pero no alcanzan ni la mitad de las correspondientes a las otras dos especies estudiadas que ecológicamente más se asemejan al charlatán: el colorín azul (Passerina cyanea), en el que ese valor asciende al 35% de los polluelos, y el gorrión corona blanca (Zonotrichia leucophrys), con un 36% de polluelos ilegítimos. Sin embargo, la proporción de vínculos poligínicos establecidos es mayor en el charlatán que en esas dos especies y esto podría permitir a los machos incrementar su éxito reproductivo más efectivamente atrayendo un mayor número de compañeras que copulando ocasionalmente con hembras desvinculadas de ellos. Los machos de charlatán proporcionan mucho más cuidado paternal a los polluelos alimentándolos que los de colorín azul y se ha demostrado que la colaboración del macho en el cuidado de los pequeños es de gran importancia para este ictérido. En consecuencia, la cantidad de polluelos ilegítimos concebidos podría ser menor entre los charlatanes machos —al menos respecto de los colorines azules— debido a que los beneficios obtenidos a través del cuidado de sus hijos podrían a menudo superar los que conseguiría involucrándose en una mayor cantidad de cópulas con hembras ajenas. Asimismo, los charlatanes se reproducen en hábitats más abiertos, lo que quizá les facilite la detección de intrusos. La sincronía en la nidificación —aparentemente más alta entre los charlatanes que entre los colorines azules y gorriones corona blanca— también reduciría las oportunidades de que se produzcan cópulas fuera de la pareja.[32]
Estado de conservación[editar]

A pesar de la tendencia negativa de su crecimiento poblacional, Birdlife International (2010) considera al charlatán una especie bajo preocupación menor debido en parte a que su población es de varios millones de ejemplares. No obstante ello, el charlatán está protegido a nivel local en algunas partes de América del Norte y ha sido declarado especie amenazada en Argentina.[4][30] En Estados Unidos y Canadá, está protegido bajo el Migratory Bird Treaty Act, y se encuentra listado como Species of Special Concern («especie de preocupación especial») en algunos estados estadounidenses.[8][37]
Crecimiento poblacional[editar]
Las fluctuaciones históricas en la cantidad de ejemplares y los cambios en su área de distribución reflejan las modificacions del paisaje y de las prácticas agrícolas. Los charlatanes anidaban originalmente en las praderas del Medio Oeste de Estados Unidos y Canadá centromeridional.[21] Su área de distribución creció hacia el este y su número aumentó gracias a la desforestación de los bosques nororientales en los siglos XVIII y XIX, ampliando los campos de heno y praderas que utilizaban para anidar.[11][21][30] Originalmente las prácticas agrícolas favorecieron la expansión del área de distribución de la mayoría de las especies de aves de pastizales en el este de Estados Unidos porque mantenían la tierra libre de vegetación leñosa.[56]
Su apogeo se produjo probablemente hacia fines del siglo XIX cuando la agricultura se expandió y el uso generalizado del caballo como medio de transporte requirió grandes extensiones de heno. Los charlatanes se beneficiaban de la floreciente industria arrocera en el sudeste de Estados Unidos antes del comienzo del siglo XX, principalmente en los estados de Georgia y Carolina del Sur. Enormes bandadas descendían sobre los arrozales para alimentarse antes de continuar su migración hacia Sudamérica. Debido a que eran capaces de producir enormes daños a los cultivos, cientos de miles de ellos fueron masacrados y servidos en restaurantes.[21]
Origen de las poblaciones occidentales[editar]
La colonización de la cuenca del lago Malheur, en el sudeste de Oregón, por parte de los charlatanes se produjo recientemente en términos relativos puesto que no fueron detectados allí en estudios llevados a cabo por Charles E. Bendire en la década de 1870. Aparentemente, no hubo en la cuenca hábitats adecuados para la especie sino hasta 1872, cuando los rancheros comenzaron a drenar las tierras anegadas para convertirlas en pasturas. Los primeros especímenes fueron recogidos en 1908 y se registró su reproducción en el lugar por primera vez en 1918. Hacia la década de 1970, la población que anidaba en el Malheur National Wildlife Refuge era la única que quedaba en el estado y, a pesar de estar confinada a un área de solo 865 hectáreas aproximadamente y no exhibir una tendencia a expandir su distribución, constituía la población más grande al oeste de las Grandes Llanuras. También se han registrado poblaciones más pequeñas en otras partes de Oregón, noreste de California —extintas en ambos casos— y otros estados y provincias canadienses occidentales. Sin embargo, el origen de las poblaciones occidentales es discutido. Tradicionalmente se ha asumido que los charlatanes colonizaron el oeste recientemente con el advenimiento de la agricultura. Por otro lado, Hamilton (1962)[9] argumentó que estas poblaciones constituirían vestigios de una antigua distribución más amplia que datara de cuando la Gran Cuenca estaba cubierta por pastizales. Aunque la población del Malheur Refuge haya resultado de una colonización reciente, esa teoría podría aún ser válida debido a que los colonizadores podrían haber surgido de otras poblaciones occidentales. No obstante, la ausencia de subespecificación entre estas poblaciones sugiere que probablemente hayan resultado de una expansión reciente en la distribución, a no ser que el flujo genético entre las poblaciones occidentales y orientales haya permanecido en niveles elevados durante largos períodos de tiempo.[45]
En 1876, Robert Ridgway comentó brevemente en una de sus obras que el charlatán «parecía estar dispersándose sobre todos los distritos del “Lejano Oeste” en donde los cultivos de cereales se habían extendido», conclusión aparentemente favorecida por el descubrimiento de individuos reproduciéndose cerca de campos de trigo en Ruby Valley (Nevada) y el registro de aves transeúntes en campos de granos cerca de Salt Lake City. Hamilton señala que esa aserción no deja en claro si Ridgway se refería a una diseminación geográfica hacia el oeste o a un crecimiento poblacional dentro de la región. En 1895 Bendire adscribió tentativamente la primera interpretación al comentario de Ridgway, y en 1939 Frederick C. Lincoln apoyó contundentemente esa postura al afirmar lo siguiente: «la expansión del área reproductiva, con el resultante cambio en la migración de la especie, ha tomado lugar desde el establecimiento del hombre blanco en el campo. Su hábitat preferido durante la temporada de nidificación son los prados húmedos y originalmente este tipo de hábitat definitivamente no podía existir en el Oeste debido a las áridas regiones existentes. Pero con la utilización de grandes áreas para el cultivo y el advenimiento de la irrigación, pequeñas colonias reproductivas de charlatanes comenzaron a aparecer en varios puntos occidentales.»[9]
Hamilton sostiene, sin embargo, que parece no haber evidencia concluyente que respalde la idea de una invasión reciente de esas áreas, pues las poblaciones occidentales incluso entonces eran pequeñas y generalmente poco conocidas. De hecho, el descubrimiento de las localizadas y restringidas poblaciones occidentales es correlativo a la exploración ornitológica del oeste. Muchos autores habían comentado sobre la sensibilidad de las poblaciones locales de charlatanes a los usos dados a la tierra y a los cambios en ellos. Es posible, según la perspectiva de Hamilton, que poblaciones locales existentes se vieran favorecidas por la llegada de la agricultura al oeste.[9]
El autor argumenta que en caso de que una tendencia a una diseminación hacia el oeste se hubiera establecido un siglo antes de sus observaciones, esta no habría seguido el ritmo del desarrollo agrícola de la región. Las poblaciones occidentales de mayor tamaño continuaban localizadas en áreas naturalmente húmedas tales como las cercanías del Malheur Refuge, en Oregón, y los alrededores del Gran Lago Salado, en Utah. Observaciones en Idaho habían confirmado que su distribución era bastante localizada aunque esparcida sobre gran parte del estado; tampoco allí los charlatanes centraban su reproducción en las proximidades de proyectos de irrigación sino que se concentraban en las inmediaciones de prados húmedos naturales. Hamilton sugiere entonces que la razón por la cual los charlatanes no se diseminaban por las áreas irrigadas en expansión del oeste yacía, en parte, en el hecho de que esas poblaciones serían en realidad remanentes poblacionales con rutas migratorias y áreas reproductivas históricas fijas. Según este autor, la naturaleza localizada de las poblaciones occidentales ciertamente apoyaría esta interpretación en lugar de apuntar a una expansión en su distribución. Debido a que la Gran Cuenca había sido en el pasado, probablemente hasta hace tan solo 11 000 años, mucho más húmeda de lo que es hoy en día, esta teoría concordaría con la historia de la región. Antaño abundaban los lagos de agua dulce y el área debió haber sido, por lo general, más húmeda y más adecuada para el charlatán. Posiblemente el charlatán habría entonces ocupado casi la totalidad de la región en donde en la actualidad subsiste en algunas zonas de manera vestigial.[9] Sin embargo, la mayoría de los ornitólogos ha defendido la teoría de una expansión reciente desde el este.[45]
Decrecimiento poblacional[editar]

Desde comienzos del siglo XX, su población se redujo, en especial en el este de Estados Unidos.[11][21][56][33] Entre las causas de su decrecimiento poblacional han sido mencionados la masacre de bandadas migratorias en los arrozales del sur de dicho país,[11] la caza comercial,[11] el abandono de las granjas,[21] la disminución de las superficies cubiertas por heno,[21][56][33] las prácticas agrícolas cambiantes, la conversión de campos en bosques y el desarrollo de los terreno agrícolas durante las décadas de 1960 y 1970,[11] su persecución en Sudamérica por su condición de plaga a través de la aplicación de plaguicidas,[4] etc. Durante el siglo XIX y a principios del siglo XX, los charlatanes eran considerados una exquisitez en el este de Estados Unidos, por lo que fueron cazados masivamente para ser vendidos en los mercados y servidos en restaurantes.[21] La extensiva caza comercial a la que fueron sometidas las bandadas otoñales a lo largo de la costa este de Estados Unidos probablemente causara el declive de las poblaciones orientales a comienzos del siglo XX.[9] Las técnicas agrícolas modernas —incluyendo rotaciones más frecuentes de los campos en los que se sembraba heno a otros cultivos,[11][33] cosechas tempranas del heno y la consecuente pérdida de nidos[4][11][33][56] y el reemplazo de pastos de estación cálida a otros de estación fresca[11]— han vuelto los terrenos agrícolas menos favorables para la reproducción del charlatán.[11] Asimismo, los campos de alfalfa (Medicago sativa), que ofrecen un hábitat reproductivo pobre a los charlatanes, han reemplazado muchos campos de fleo de los prados (Phleum pratense) y fabáceas.[11][21][56] La pérdida de su hábitat es en gran parte responsable por el decrecimiento de las poblaciones en Estados Unidos.[11] Adicionalmente, el hecho de que en la actualidad los cultivos se cosechen más temprana y frecuentemente y el empleo de maquinaria moderna causan la muerte de muchas aves jóvenes.[7][21][30] Además, en Argentina es habitual su captura y su posterior venta como mascota, actividad que data desde al menos principios del siglo XX.[37]
Según datos de la North American Breeding Bird Survey, los números de charlatanes han estado disminuyendo significativamente desde 1966 a lo largo de toda su área reproductiva; entre 1980 y 1996, la tasa anual de decrecimiento poblacional fue del 3,8%.[37] La información de la Breeding Bird Survey, basada en observaciones de campo, señala un descenso de más del 90% en la población de charlatanes entre 1966 y 1992 en un área de 37 000 km² del norte de Illinois, el cual podría estar relacionado con una disminución en la superficie cubierta de pasturas, alfalfa y avenas en la zona.[57]
En Sudamérica, la concentración de la población en unas pocas zonas agrícolas —mayormente arroceras— de Bolivia, Paraguay y Argentina los hace vulnerables a los cambios provocados por la actividad humana y a las catástrofes naturales. Sumado a la amenaza que representa dicho hábito gregario, cabe destacar el hecho de que son percibidos como plagas y combatidos por los agricultores del arroz, ya que suelen mezclarse con otros ictéridos como los varilleros congos (Chrysomus ruficapillus) o los renegridos (Molothrus bonariensis), que se ven favorecidos por la presencia de los cultivos y se han transformados en verdaderas plagas.[4] Se han registrado muertes de charlatanes debido a la utilización del pesticida organofosforado clorpirifós. Las aplicaciones aéreas con ingredientes altamente tóxicos —por ejemplo, malatión y monocrotofós— para controlar las cantidades de aves dañinas por parte de productores de arroz parecen haber disminuido en algunas áreas, pero siguen siendo llevadas a cabo en otras a fin de mitigar los perjuicios ocasionados por los varilleros congos, lo cual afecta indirectamente a los charlatanes.[8] Cabe destacar que el charlatán parece tener un impacto sobre los cultivos de arroz mucho menor al percibido por los agricultores.[36] Por otro lado, son ahora considerados beneficiosos para la agricultura en Estados Unidos y Canadá, debido a que el grueso de su dieta durante la época de reproducción está constituido por insectos, muchos de los cuales son dañinos para los cultivos.[21][30] Además, la mayor parte de los alimentos vegetales que consumen durante esos meses son semillas de hierbas o de plantas sin valor comercial.[21]
Notas[editar]
- ↑ Es denominado chupador en las arroceras de Argentina debido a su hábito de exprimir el arroz en estado lechoso, que refiere al período en el que se forman las semillas.
Referencias[editar]
- ↑ a b c BirdLife International (2012). «Dolichonyx oryzivorus». Lista Roja de especies amenazadas de la UICN 2013.2 (en inglés). ISSN 2307-8235. Consultado el 16 de mayo de 2014.
- ↑ Zoonomen. «Birds of the World -- current valid scientific avian names» (en inglés). Consultado el 29 de noviembre de 2011.
- ↑ a b c d The Taxonomicon. «Dolichonyx oryzivorus (C. Linnaeus, 1758) - bobolink» (en inglés). Consultado el 29 de noviembre de 2011.
- ↑ a b c d e f g h i j k l m n ñ o p q r s t u v w x y z aa ab López-Lanús, Bernabé; Marino, Gustavo D., eds. (2010). Aportes al conocimiento de la ecología del Charlatán y su estado actual en la Provincia de Santa Fe, Argentina. Temas de Naturaleza y Conservación, Monografía de Aves Argentinas N° 7. Buenos Aires (Argentina): Aves Argentinas / Asociación Ornitológica del Plata. ISBN 978-987-26580-0-7. Archivado desde el original el 4 de marzo de 2016. Consultado el 28 de noviembre de 2011.
- ↑ De Juana, E; Del Hoyo, J; Fernández-Cruz, M; Ferrer, X; Sáez-Royuela, R; Sargatal, J (2012). «Nombres en castellano de las aves del mundo recomendados por la Sociedad Española de Ornitología (Decimosexta parte: Orden Passeriformes, Familias Thraupidae a Icteridae)». Ardeola. Handbook of the Birds of the World (Madrid: SEO/BirdLife) 59 (1): 157-166. ISSN 0570-7358. Consultado el 5 de mayo de 2019.
- ↑ Perlut, Noah G. (3 de junio de 2008). «Female bobolink molts into male-like plumage and loses fertility». Journal of Field Ornithology (en inglés) (Association of Field Ornithologists) 79 (2): 198-201. Consultado el 23 de diciembre de 2011.
- ↑ a b c d e f g h i j k l m n ñ o p «Bobolink». All About Birds (en inglés). Ithaca (Nueva York): Cornell Lab of Ornithology. Consultado el 29 de diciembre de 2010.
- ↑ a b c López-Lanús, Bernabé; Roesler, Ignacio; Blanco, Daniel E.; Petracci, Pablo F.; Serra, María; Zaccagnini, María Elena (2007). «Bobolink (Dolichonyx oryzivorus) numbers and non breeding ecology in the rice fields of San Javier, Santa Fe Province, Argentina». Ornitología Neotropical (en inglés) (Sociedad Ornitológica Neotropical) 18: 493-502. Consultado el 5 de diciembre de 2011. (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última).
- ↑ a b c d e f g h i j k l m n ñ o p q r Hamilton, William J., III (abril de 1962). «Bobolink migratory pathways and their experimental analysis under night skies». The Auk (en inglés) (American Ornithologists' Union) 79 (2): 208-233. Consultado el 24 de noviembre de 2011.
- ↑ a b c Beason, Robert C. (julio de 1987). «Interaction of visual and non-visual cues during migratory orientation by the bobolink (Dolichonyx oryzivorus)». Journal of Ornithology (en inglés) (Springer-Verlag) 128 (3): 317-324. Consultado el 24 de noviembre de 2011.
- ↑ a b c d e f g h i j k l m n ñ o p «New Jersey - Bobolink, Dolichonyx oryzivorus.» (en inglés). Consultado el 29 de diciembre de 2010.
- ↑ a b c d e f g h i j k l m n ñ o p q r s t Martin, Stephen G. (1974). «Adaptations for polygynous breeding in the bobolink, Dolichonyx oryzivorus.». American Zoologist (en inglés) (American Society of Zoologists) 14 (1): 109-119. Consultado el 30 de diciembre de 2010.
- ↑ Boyd, John H., III (14 de septiembre de 2011). «CORE PASSEROIDEA III – Calcariidae, Lamprospizidae, Parulidae, Icteridae». TiF Checklist (en inglés). Consultado el 10 de marzo de 2012.
- ↑ Linneo, Carlos (1758). Laurentii Salvii, ed. Systema naturæ per regna tria naturæ, secundum classes, ordines, genera, species, cum characteribus, differentiis, synonymis, locis (en latín). Tomo 1 (décima edición). Salvius publ. p. 179. Consultado el 5 de diciembre de 2011.
- ↑ a b Coues, Elliott; Allen, J. A.; Brewster, William; Merriam, C. Hart; Ridgway, Robert (enero de 1894). «Sixth supplement to the American Ornithologists' Union check-list of North American birds». The Auk (en inglés) (American Ornithologists' Union) 11 (1): 46-51. Consultado el 8 de diciembre de 2011.
- ↑ a b c d e f g h Chapman, Frank M. (enero de 1890). «On the winter distribution of the bobolink (Dolichonyx oryzivorus) with remarks on its routes of migration». The Auk (en inglés) (American Ornithologists' Union) 7 (1): 39-45. Consultado el 8 de diciembre de 2011.
- ↑ Clements, J. F.; Schulenberg, T. S.; Iliff, M. J.; Sullivan, B. L.; Wood, C. L.; Roberson, D. (2011). The Clements checklist of birds of the world: Version 6.6. (en inglés). Cornell Lab of Ornithology. Archivado desde el original el 6 de enero de 2012. Consultado el 13 de diciembre de 2011.
- ↑ a b c d e f g h i «Bobolinks, Dolichonyx oryzivorus: Information and Photos» (en inglés). Avian Web. Archivado desde el original el 17 de agosto de 2010. Consultado el 30 de diciembre de 2010.
- ↑ MacKenzie, Hall (2008). «The Endagered Species Spotlight - Bobolink». Tracks (en inglés) (Trenton (Nueva Jersey): Conserve Wildlife Foundation of New Jersey) 1 (2): 1-2. Consultado el 4 de enero de 2011.
- ↑ Chapman, Frank M. (abril de 1897). «Remarks on the spring moult of the bobolink». The Auk (en inglés) (American Ornithologists' Union) 14 (2): 149-154. Consultado el 9 de diciembre de 2011.
- ↑ a b c d e f g h i j k l m n ñ o p q r s t u v w x y Deinlein, Mary (febrero de 1997). «Smithsonian Migratory Bird Center: Bobolink» (en inglés). Instituto Smithsoniano. Archivado desde el original el 9 de marzo de 2011. Consultado el 28 de diciembre de 2010.
- ↑ a b c d e f Howell, S. N. G.; Webb, S. (1995). A Guide to the Birds of Mexico and Northern Central America (en inglés). Oxford (Inglaterra): Oxford University Press. ISBN 978-0198540120. Consultado el 5 de enero de 2012.
- ↑ Chapman, Frank M. (abril de 1890). «On the changes of plumage in the bobolink (Dolichonyx oryzivorus)». The Auk (en inglés) (American Ornithologists' Union) 7 (2): 120-124. Consultado el 9 de diciembre de 2011.
- ↑ a b c d «Bobolink - Bird Web» (en inglés). Seattle Audubon Society. Consultado el 30 de diciembre de 2010.
- ↑ a b c d e f g h i j k l m n ñ Wittenberger, James F. (febrero de 1982). «Factors affecting how male and female bobolinks apportion parental investments». The Condor (en inglés) (Cooper Ornithological Society) 84 (1): 22-39. Consultado el 26 de diciembre de 2011. (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última).
- ↑ a b c Schulenberg, T. S.; Stotz, D. F.; Lane, D. F.; O'Neill, J. P.; Parker, T. A., III (2008). Birds of Peru (en inglés). Princeton (Nueva Jersey): Princeton University Press. ISBN 978-0-7136-8673-9.
- ↑ a b Gavin, Thomas A. (enero de 1984). «Broodedness in bobolinks». The Auk (en inglés) (American Ornithologists' Union) 101 (1): 179-181. Consultado el 24 de diciembre de 2011.
- ↑ a b «Mystery Bird: Bobolink, Dolichonyx oryzivorus.». Punctuated Equilibrium (en inglés). The Guardian. Consultado el 29 de diciembre de 2010.
- ↑ a b Blanco, D. E.; López-Lanús, B., eds. (2008). Introducción de Ecología no reproductiva y conservación del Charlatán (Dolichonyx oryzivorus) en noreste de Argentina.. Buenos Aires (Argentina): Fundación Humedales / Wetlands International. ISBN 978-987-24710-0-2. Archivado desde el original el 7 de julio de 2010. Consultado el 30 de diciembre de 2010.
- ↑ a b c d e f g h i j Van Damme, Linda M. (marzo de 1999). «Status of the bobolink in British Columbia». Wildlife Working Report (en inglés) (Victoria (Columbia Británica): Ministry of Environment, Lands and Parks of British Columbia, Wildlife Branch) (WR-93): 1-11. ISBN 0-7726-3845-4. Archivado desde el original el 24 de septiembre de 2015. Consultado el 30 de diciembre de 2011.
- ↑ a b c d e f Gavin, Thomas A.; Bollinger, Eric K. (julio de 1985). «Multiple paternity in a territorial passerine: The bobolink». The Auk (en inglés) (American Ornithologists' Union) 102 (3): 550-555. Consultado el 26 de diciembre de 2011.
- ↑ a b c d e f g h i j k l Bollinger, Eric K.; Gavin, Thomas A. (agosto de 1991). «Patterns of extra-pair fertilizations in bobolinks». Behavioral Ecology and Sociobiology (en inglés) (Springer-Verlag) 29 (1): 1-7. Consultado el 23 de diciembre de 2011.
- ↑ a b c d e Bollinger, E. K.; Gavin, T. A. (1992). «Eastern bobolink populations: Ecology and conservation in an agricultural landscape». En Hagan, J. M.; Johnston, D. W., eds. Ecology and conservation of neotropical migrant landbirds (en inglés). Washington D. C.: Smithsonian Institution Press. Consultado el 11 de octubre de 2011. (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última).
- ↑ Fletcher, Robert J. Jr.; Koford, Rolf R. (julio de 2003). «Spatial responses of bobolinks (Dolichonyx oryzivorus) near different types of edges in northern Iowa». The Auk (en inglés) (American Ornithologists' Union) 120 (3): 799-810. Consultado el 22 de noviembre de 2011.
- ↑ Bollinger, Eric K.; Gavin, Thomas A. (julio de 2004). «Responses of nesting bobolinks (Dolichonyx oryzivorus) to habit edges». The Auk (en inglés) (American Ornithologists' Union) 121 (3): 767-776. Consultado el 23 de noviembre de 2011.
- ↑ a b c d e f g h i j Renfrew, Rosalind B.; Saavedra, Ana María (2007). «Ecology and conservation of bobolinks (Dolichonyx oryzivorus) in rice production regions of Bolivia». Ornitología Neotropical (en inglés) (Sociedad de Ornitología Neotropical) 18: 61-73. Archivado desde el original el 13 de diciembre de 2013. Consultado el 5 de diciembre de 2011.
- ↑ a b c d e f g h i Di Giacomo, Adrián S.; Di Giacomo, Alejandro G.; Contreras, Julio R. (2005). «Status and conservation of the bobolink (Dolichonyx oryzivorus) in Argentina». USDA Forest Service General Technical Report PSW-GTR-191 (en inglés) (Albany (California): Pacific Southwest Research Station, Servicio Forestal de los Estados Unidos, Departamento de Agricultura): 519-524. Consultado el 4 de diciembre de 2011. (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última).
- ↑ a b c «Bobolink Dolichonyx oryzivorus.» (en inglés). eNature. Archivado desde el original el 2 de enero de 2010. Consultado el 30 de diciembre de 2010.
- ↑ a b c d e f Capp, Michael S.; Searcy, William A. (marzo de 1991). «An experimental study of song type function in the bobolink (Dolichonyx oryzivorus)». Behavioral Ecology and Sociobiology (en inglés) (Springer-Verlag) 28 (3): 179-186. Consultado el 9 de agosto de 2011.
- ↑ a b c d e f g h Capp, Michael S. (mayo de 1992). «Tests of the function of the song repertoire in bobolinks». The Condor (en inglés) (Cooper Ornithological Society) 94 (2): 468-479. Consultado el 20 de diciembre de 2011.
- ↑ Capp, Michael S.; Searcy, William A. (1991). «Acoustical communication of aggressive intentions by territorial male bobolinks». Behavioral Ecology (en inglés) (International Society for Behavioral Ecology) 2 (4): 319-326. Consultado el 21 de diciembre de 2011.
- ↑ Ammer, Frank K.; Capp, Michael S. (agosto de 1999). «Song versatility and social context in the bobolink». The Condor (en inglés) (Cooper Ornithological Society) 101 (3): 686-688. Consultado el 21 de diciembre de 2011.
- ↑ a b «Grassland Birds: Bobolink» (en inglés). The Nature Conservancy. Archivado desde el original el 9 de noviembre de 2013. Consultado el 29 de diciembre de 2010.
- ↑ a b Rodenhouse, Nicholas L.; Best, Louis B.; O'Connor, Raymond J.; Bollinger, Eric K. (21-25 de septiembre de 1992). «Effects of temperate agriculture on neotropical migrant landbirds». General Technical Report RM-229 (en inglés) (Fort Collins (Colorado): Departamento de Agricultura de Estados Unidos, Servicio Forestal, Rocky Mountain Forest and Range Experiment Station): 280-295. Consultado el 4 de abril de 2011.
- ↑ a b c Wittenberger, James F. (invierno de 1978). «The breeding biology of an isolated bobolink population in Oregon». The Condor (en inglés) (Cooper Ornithological Society) 80 (4): 355-371. Consultado el 20 de octubre de 2011.
- ↑ a b c d e f g h i j k l Wittenberger, James F. (septiembre de 1980). «Feeding of secondary nestlings by polygynous male bobolinks in Oregon». The Wilson Bulletin (en inglés) (Wilson Ornithological Society) 92 (3): 330-340. Consultado el 10 de julio de 2011.
- ↑ «Bobolink Dolichonyx oryzivorus.» (en inglés). Servicio Geológico de los Estados Unidos. Consultado el 31 de diciembre de 2010.
- ↑ «Brown-headed cowbirds in grasslands: Their habitats, hosts, and response to management» (en inglés). Departamento de Interior de los Estados Unidos, Servicio Geológico, Northern Prairie Wildlife Research Center. 3 de agosto de 2006, fecha de última modificación cuando la página fue consultada. Archivado desde el original el 22 de junio de 2010. Consultado el 10 de febrero de 2011.
- ↑ a b Friedmann, Herbert; Kiff, Lloyd F.; Rothstein, Stephen I. (1977). «Brown-headed Cowbird (Molothrus ater)». A further contribution to knowledge of the host relations of the parasitic cowbirds (en inglés). Smithsonian Contributions to Zoology, n° 235. Washington D.C.: Smithsonian Institution Press. pp. 5-51. Consultado el 26 de junio de 2011.
- ↑ a b c Gavin, Thomas A.; Bollinger, Eric K. (febrero de 1988). «Reproductive correlates of breeding-site fidelity in bobolinks (Dolichonyx oryzivorus)». Ecology (en inglés) (Ecological Society of America) 69 (1): 96-103. Consultado el 16 de noviembre de 2011.
- ↑ Bollinger, Eric K.; Gavin, Thomas A. (octubre de 1989). «The effects of site quality on breeding-site fidelity in bobolinks». The Auk (en inglés) (American Ornithologists' Union) 106 (4): 584-594. Consultado el 22 de noviembre de 2011.
- ↑ Mather, Monica H.; Robertson, Raleigh J. (octubre de 1992). «Honest advertisement in flight displays of bobolinks (Dolichonyx oryzivorus)». The Auk (en inglés) (American Ornithologists' Union) 109 (4): 869-873. Consultado el 27 de noviembre de 2011.
- ↑ a b c Moskwik, Matthew P.; O’Connell, Margaret A. (2006). «Male and female reproductive strategies in the polygynous bobolink». Norwest Science (en inglés) (Norwest Scientific Association) 80 (2): 108-115. Archivado desde el original el 25 de noviembre de 2013. Consultado el 22 de diciembre de 2011.
- ↑ a b Granfors, Diane A.; Pietz, Pamela J.; Joyal, Lisa A. (julio de 2001). «Frequency of egg and nestling destruction by female brown-headed cowbirds at grassland nests». The Auk (en inglés) (American Ornithologists' Union) 118 (3): 765-769. Consultado el 21 de diciembre de 2011.
- ↑ Robertson, Raleigh J.; Norman, Richard F. (verano de 1976). «Behavioral defenses to brood parasitism by potential hosts of the brown-headed cowbird». The Condor (en inglés) (Cooper Ornithological Society) 78 (2): 166-173. Consultado el 8 de octubre de 2011.
- ↑ a b c d e Bollinger, Eric K.; Blair Bollinger, Patricia; Gavin, Thomas A. (verano de 1990). «Effects of hay-cropping on eastern populations of the bobolink». Wildlife Society Bulletin (en inglés) (Allen Press) 18 (2): 142-150. Consultado el 12 de octubre de 2011.
- ↑ Herkert, James R. (abril de 1997). «Bobolink Dolichonyx oryzivorus population decline in agricultural landscapes in the Midwestern USA». Biological Conservation (en inglés) 80 (1): 107-112. Consultado el 17 de noviembre de 2011.
Enlaces externos[editar]
 Wikimedia Commons alberga una categoría multimedia sobre Dolichonyx oryzivorus.
Wikimedia Commons alberga una categoría multimedia sobre Dolichonyx oryzivorus. Wikispecies tiene un artículo sobre Dolichonyx oryzivorus.
Wikispecies tiene un artículo sobre Dolichonyx oryzivorus.- Vocalizaciones del charlatán, en YouTube. Producido en cooperación con The Music of Nature © 2010, Lang Elliott y Bob McGuire.
- El contenido de este artículo incorpora traducciones de las obras Chapman on the Winter Distribution of the Bobolink y de Factors affecting how male and female boblink apportion parental investmets.

